В последние годы отмечается устойчивый рост числа пациентов с тикозными расстройствами1. Каковы механизмы этого феномена и почему именно вечерние часы становятся периодом увеличения симптомов?
Прежде всего необходимо определить основные звенья патогенеза и вовлеченные в процесс формирования тиков структуры мозга:


Почему тики усиливаются в вечернее время суток?
Ответ кроется в нарушении уровня нейромедиаторов и гормонов, которые регулируют активность на протяжении дня:
Дисрегуляция уровня кортизола:
Нарушение секреции кортизола может усиливать тики4
Нарушение циркадных ритмов и уровня дофамина:
Дофаминергическая дисрегуляция может влиять на циркадные ритмы и время проявления тиков5
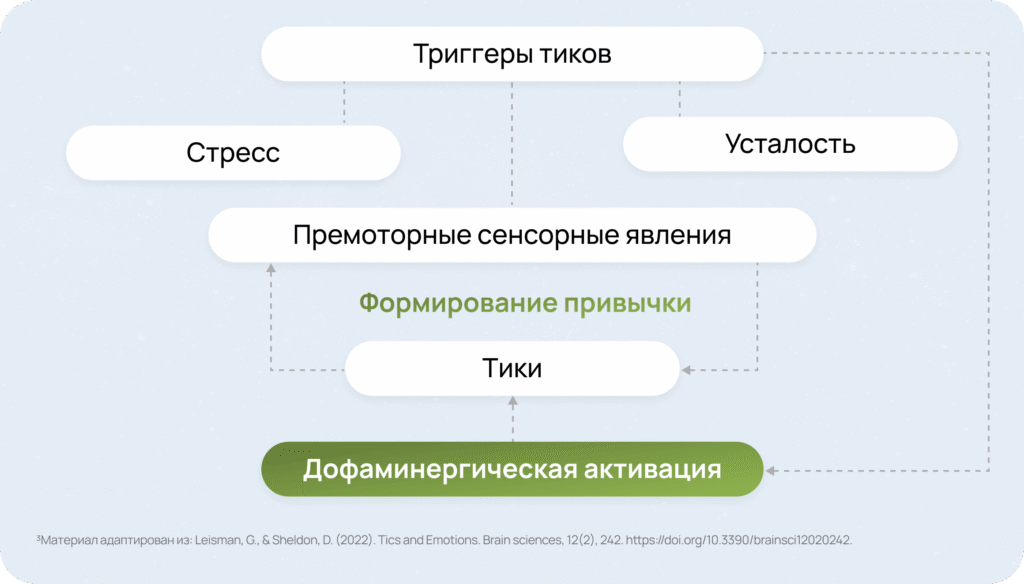
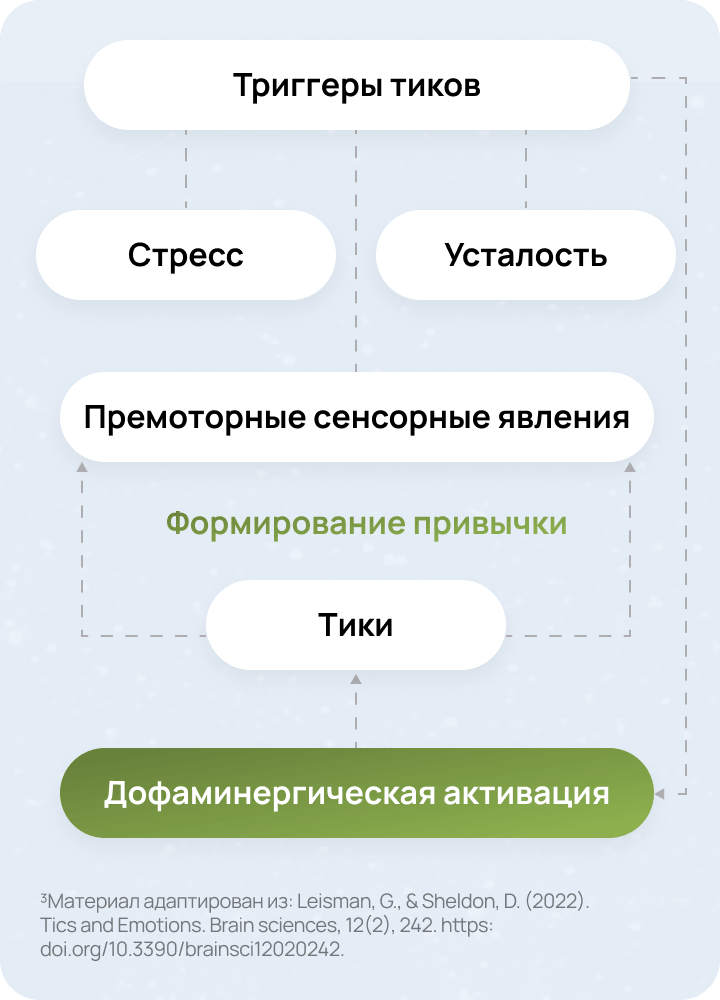
Стресс и усталость в формировании тиков3
Тики формируются в результате высокой сенсорной стимуляции, вызванной стрессом, усталостью и другими триггерами3
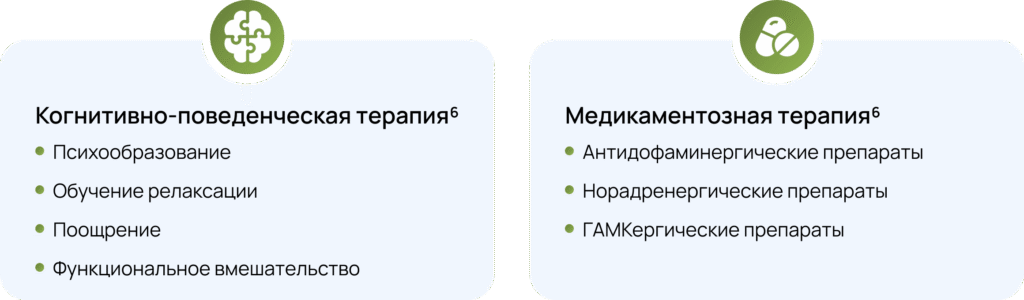
Подходы к лечению тиков
Современное лечение тиков предполагает комплексную стратегию, объединяющую немедикаментозные и медикаментозные подходы.

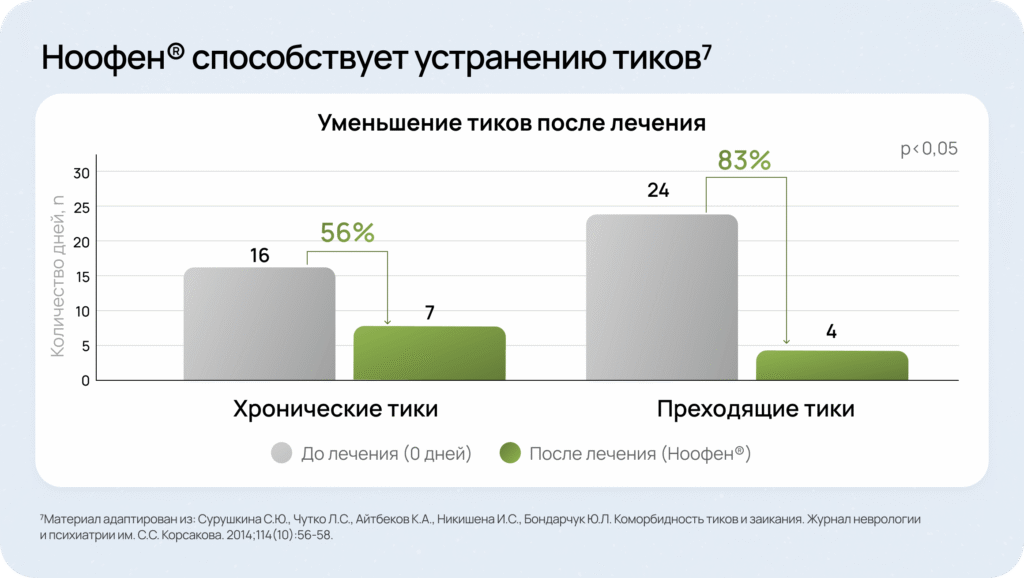




- Tang, N., Wang, Y., Jiang, X., Liu, H., Li, Y., Qu, J., & Xiang, S. (2025). Clinical characteristics of tic disorders in children and adolescents with the chief complaint of abnormal blinking. Frontiers in psychiatry, 16, 1553358. https://doi.org/10.3389/fpsyt.2025.1553358.
- Ueda, K., & Black, K. J. (2021). A Comprehensive Review of Tic Disorders in Children. Journal of Clinical Medicine, 10(11), 2479. https://doi.org/10.3390/jcm10112479.
- Leisman, G., & Sheldon, D. (2022). Tics and Emotions. Brain sciences, 12(2), 242. https://doi.org/10.3390/brainsci12020242.
- B.A. Corbett, S.P. Mendoza, C.L. Baym, S.A. Bunge, S. Levine. (2008). Examining cortisol rhythmicity and responsivity to stress in children with Tourette syndrome. Psychoneuroendocrinology,33(6),810-820. https://doi.org/10.1016/j.psyneuen.2008.03.014.
- Ricketts, E. J., Montalbano, G. E., Burgess, H. J., McMakin, D. L., Coles, M. E., Piacentini, J., & Colwell, C. S. (2022). Sleep and chronotype in adults with persistent tic disorders. Journal of clinical psychology, 78(7), 1516-1539. https://doi.org/10.1002/jclp.23323.
- Desai, I., Kumar, N., & Goyal, V. (2023). An Update on the Diagnosis and Management of Tic Disorders. Annals of Indian Academy of Neurology, 26(6), 858–870. https://doi.org/10.4103/aian.aian_724_23.
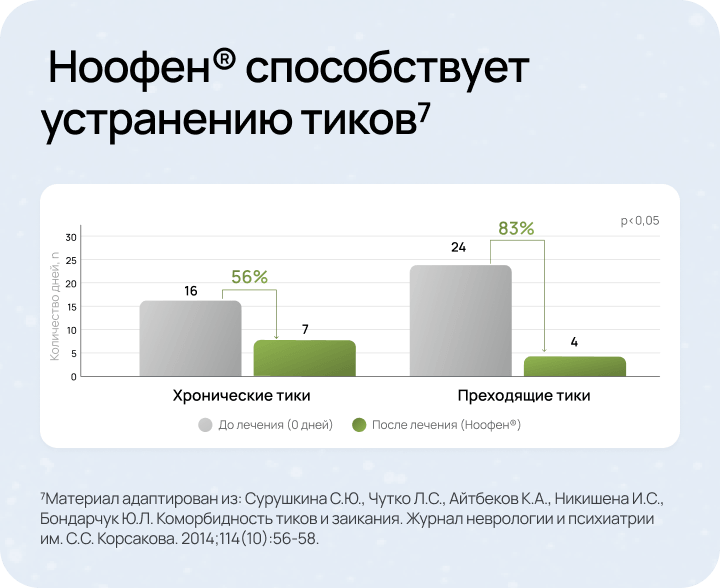
- Сурушкина С.Ю., Чутко Л.С., Айтбеков К.А., Никишена И.С., Бондарчук Ю.Л. Коморбидность тиков и заикания. Журнал неврологии и психиатрии им. С.С. Корсакова. 2014;114(10):56‑58.
- Инструкция по медицинскому применению препарата Ноофен®, капсулы 500 мг.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Энурез — самая распространенная причина функционального недержания мочи у детей
Понимание эпидемиологии позволяет объективно оценивать масштаб проблемы и выявлять группы риска1.

Для эффективного лечения энуреза критически важно понимать его этиологию. Современные исследования выделяют несколько ключевых факторов развития этого состояния, среди которых особое место занимает генетическая предрасположенность2.

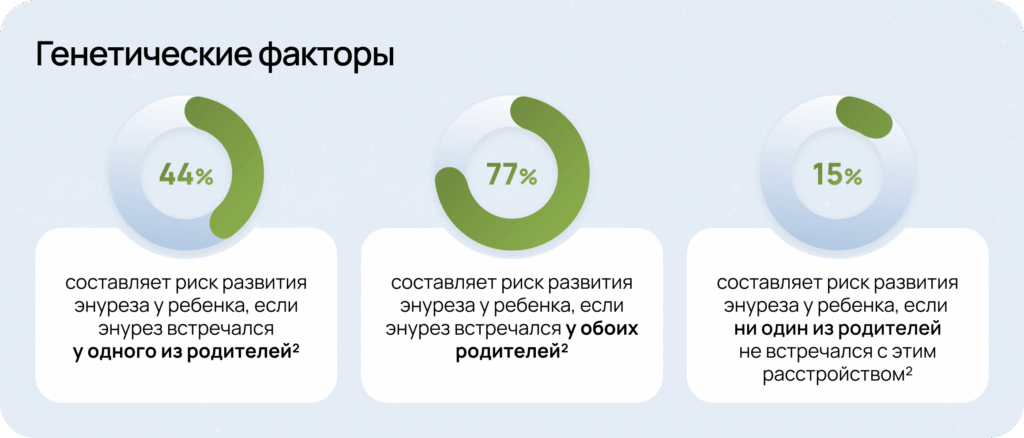
Основная причина энуреза — невозможность выработки рефлекса пробуждения на сигнал от наполненного мочевого пузыря. Это связано с задержкой созревания нервно-гуморальных структур3.
Подходы к диагностике энуреза2,4
Прежде всего необходимо определить тип энуреза (первичный/вторичный, а также моносимптомный/полисимптомный) и убедиться в соответствии клинической картины диагностическим критериям. Существует четкая систематизация форм энуреза, которая определяет дальнейшую тактику ведения пациента2:
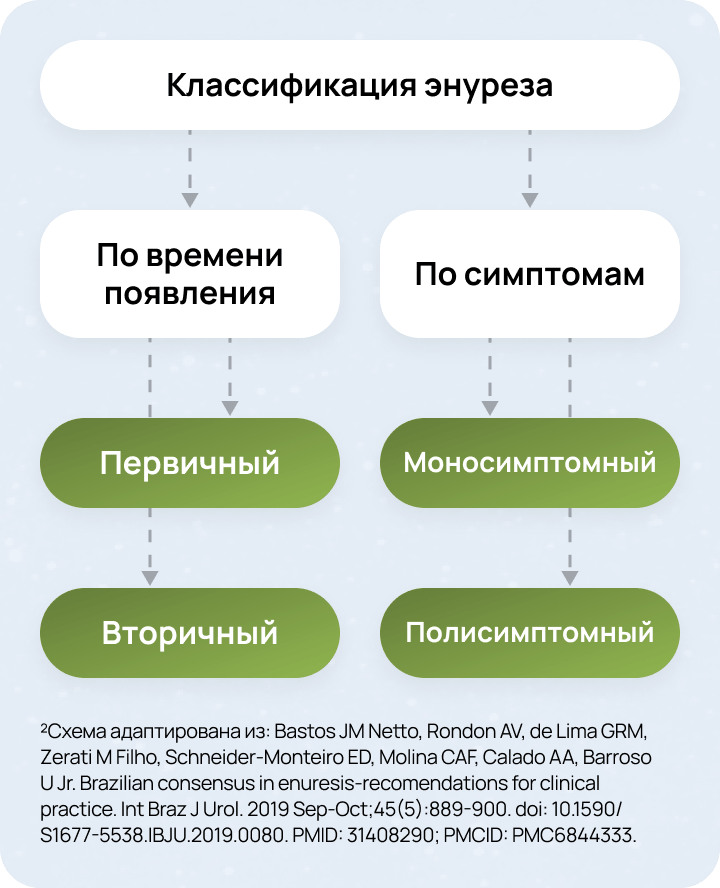
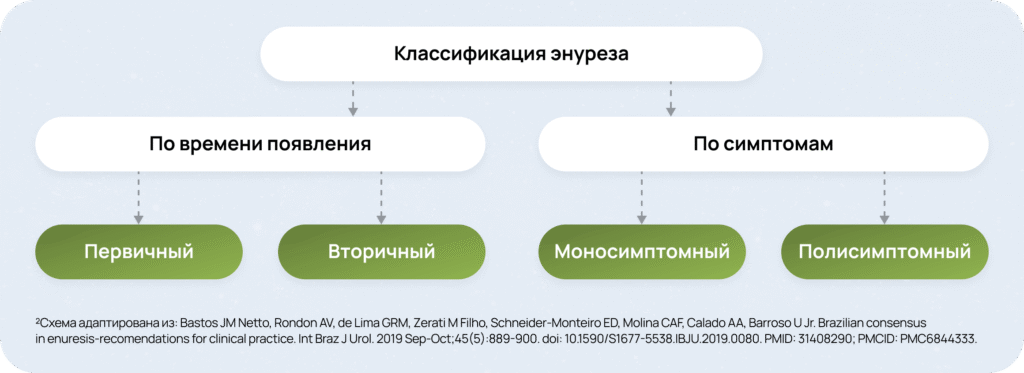
- Первичный энурез
Непроизвольное мочеиспускание во время сна у ребенка 5-ти лет и старше без «сухих» промежутков длительностью до 6 месяцев4
- Вторичный энурез
Непроизвольное мочеиспускание во время сна у ребенка старше 5-ти лет, после полностью «сухих» ночей в течение периода длительнее, чем 6 месяцев4
- Моносимптомный энурез
Непроизвольное мочеиспускание во время сна у ребенка 5 лет и старше при отсутствии других признаков расстройств мочеиспускания4
- Полисимптомный энурез
Непроизвольное мочеиспускание во время сна у ребенка с другими признаками расстройств нижних мочевых путей4


Комплексная терапия энуреза2,4
Современный подход к терапии энуреза предполагает комплексную стратегию, включающую немедикаментозные и медикаментозные методы. Важно понимать, что успешная коррекция энуреза достигается не одним универсальным методом, а грамотным сочетанием различных терапевтических подходов.




Оптимальным решением для медикаментозной терапии энуреза может выступать аминофенилмасляная кислота (например, препарат Ноофен®).
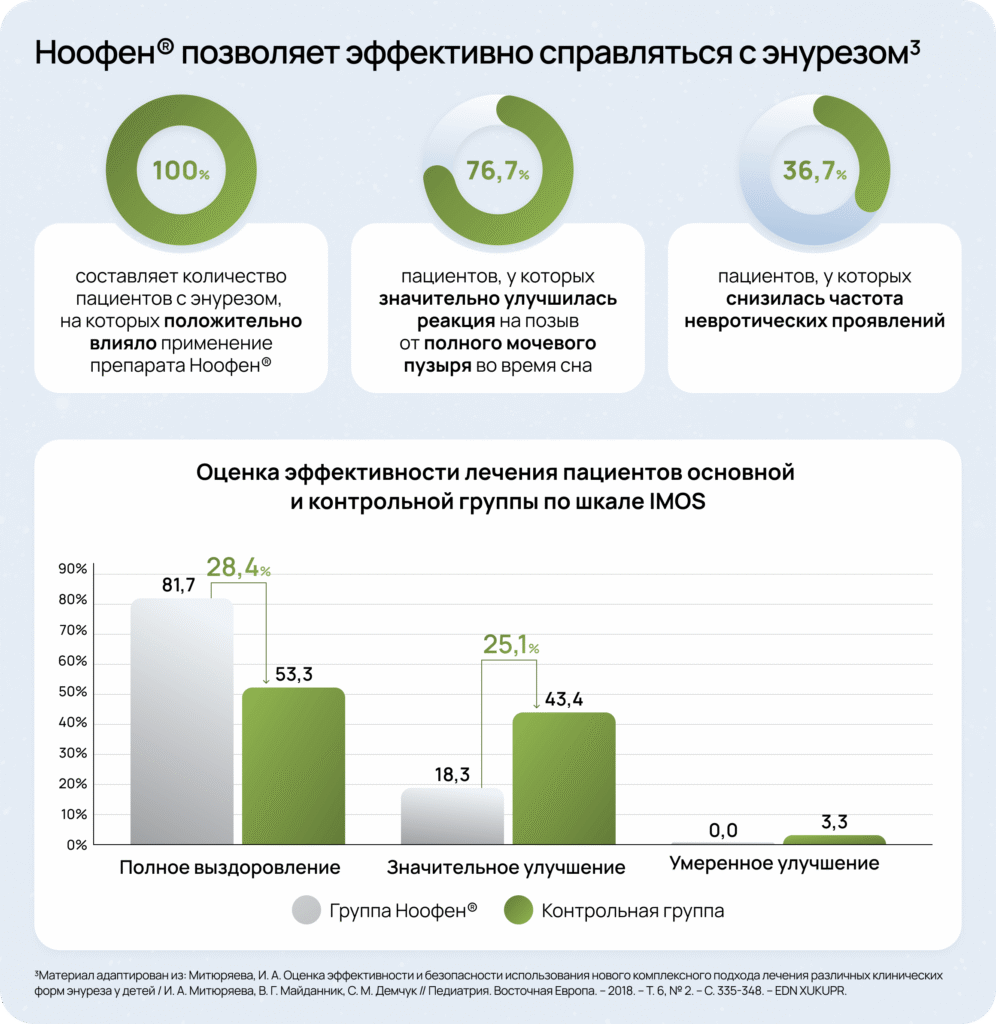
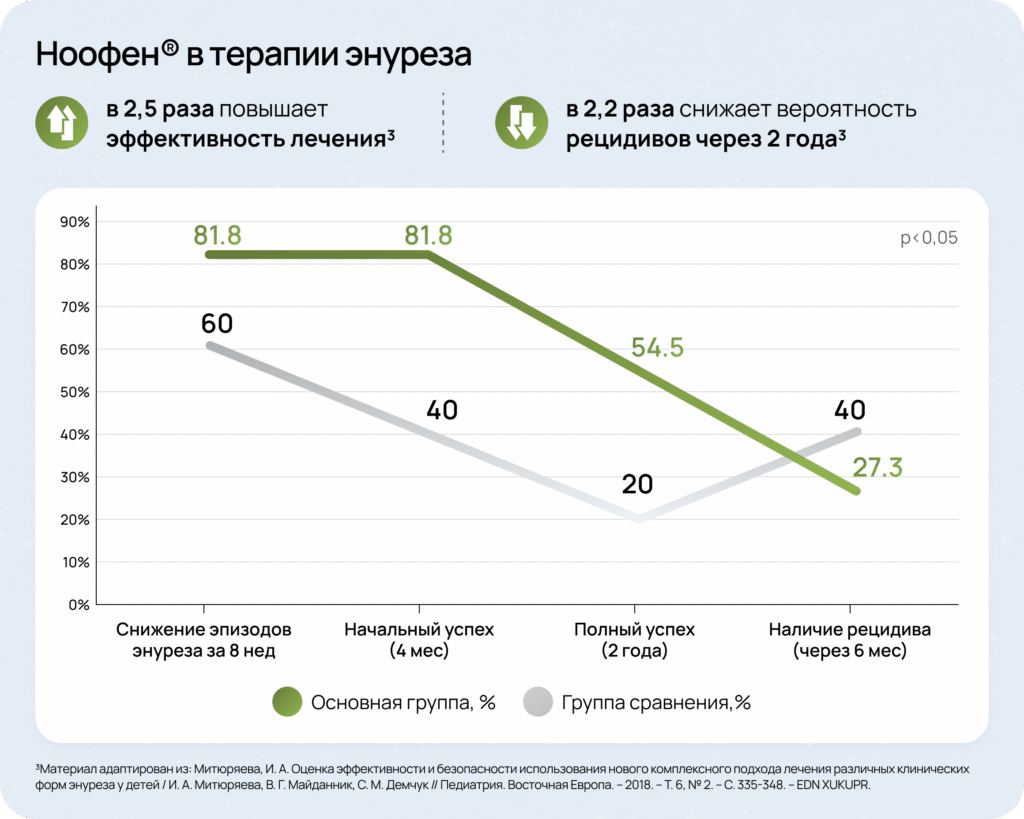


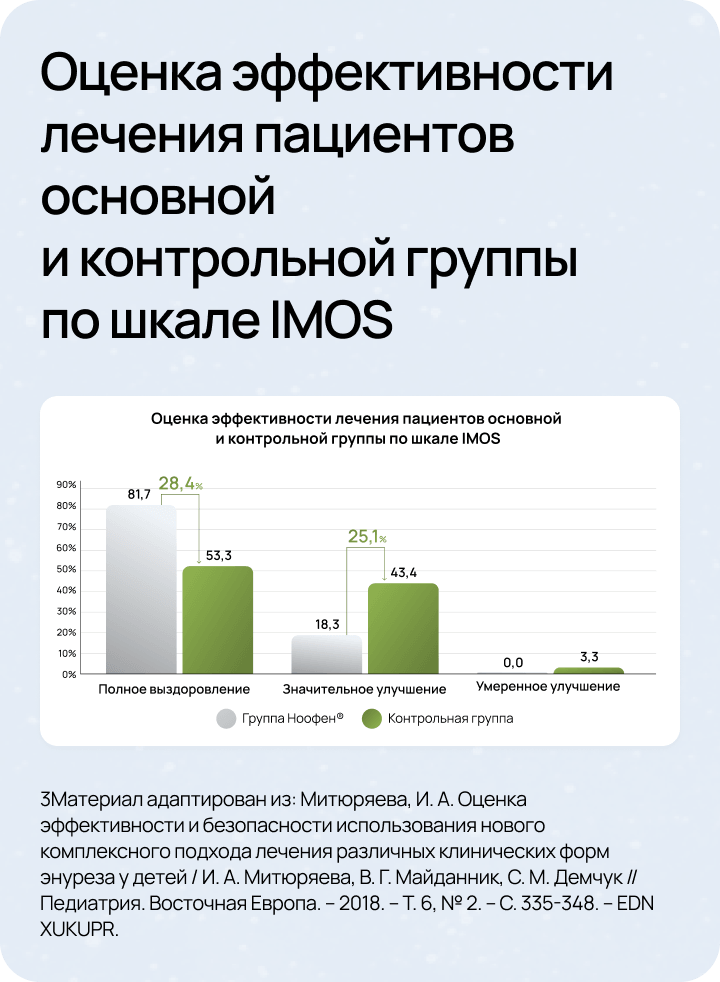
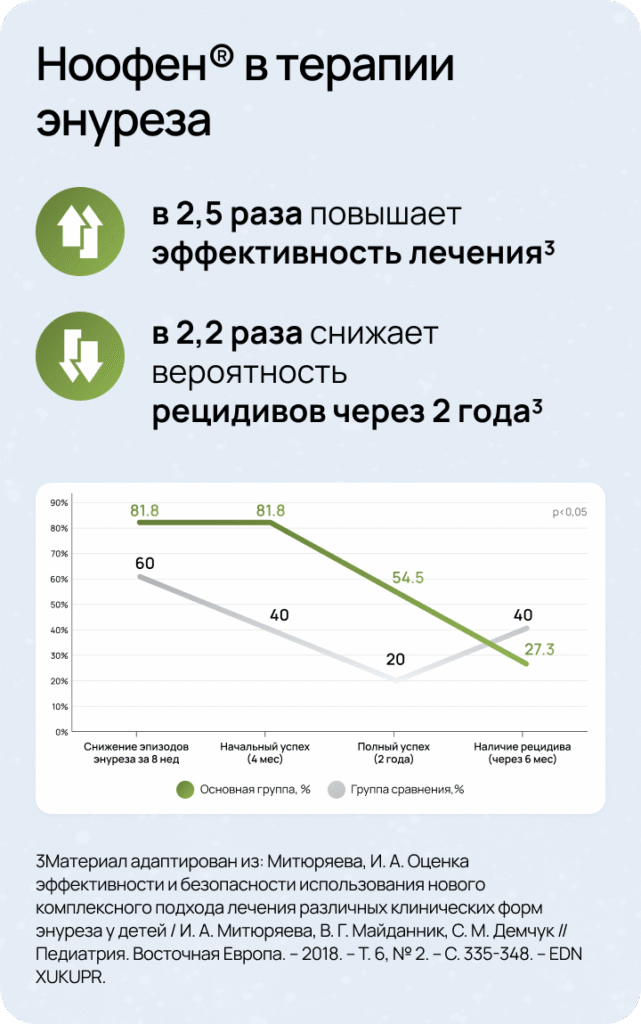

- Pole, R., Vankar, G. K., and Ghogare, A. S. (2022). A clinical review of enuresis andits associated psychiatric comorbidities. Ann. Indian Psychiatry 6, 4-14. doi: 10.4103/aip.aip_102_21.
- Bastos JM Netto, Rondon AV, de Lima GRM, Zerati M Filho, Schneider-Monteiro ED, Molina CAF, Calado AA, Barroso U Jr. Brazilian consensus in enuresis-recomendations for clinical practice. Int Braz J Urol. 2019 Sep-Oct;45(5):889-900. doi: 10.1590/S1677-5538.IBJU.2019.0080. PMID: 31408290; PMCID: PMC6844333.
- Митюряева И.А., Майданник В.Г., Демчук С.М. Оценка эффективности и безопасности использования нового комплексного подхода лечения различных клинических форм энуреза у детей. Педиатрия. Восточная Европа. 2018; 6(2):335-348.
- Алгоритмы диагностики и лечения детей с расстройствами мочеиспускания неорганического генеза (без пороков и травм позвоночника и спинного мозга). Алгоритмы разработаны на базе московского городского центра детской урологии, андрологии и патологии тазовых органов ГБУЗ «Детская городская больница №9 им. Г.Н. Сперанского ДЗМ», отдела хирургии детского возраста ФГБОУ ВО РНИМУ им. Н.И. Пирогова НПЦ детской психоневрологии ДЗ г. Москвы на основании стандартов ICCS/Гусева Н.Б.- Москва,2020. — 30 с.
- Taborga Díaz, E., Martínez Suárez, V., Alcántara-Canabal, L., Suárez Castañón, C., & Cebrián Muíños, C. (2021). Assessment of nocturnal enuresis diagnostic criteria. Anales de pediatria, 95(2), 101–107. https://doi.org/10.1016/j.anpede.2020.08.005.
- Инструкция по медицинскому применению лекарственного средства Ноофен®, капсулы 500 мг.
- Mehilane L.S., RyagoL.K., AllikmetsL.Kh. Farmokologiya i Klinika Fenibuta. Tartu State University, Department of Pharmacology, 1990.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Эффективность под угрозой: что показало исследование 6 образцов фенибута
Идентичные на первый взгляд молекулы могут радикально отличаться по качеству, биодоступности и безопасности, что определяется стандартами производства, контролем сырья и технологическими процессами на этапах создания препарата.
В новом исследовании было проанализировано 6 аналогов оригинального фенибута (Ноофен®), приобретенных онлайн. Результаты оказались тревожными1:


Клинические риски1:
- Реальное количество потребленного фенибута, приобретенного у неизвестного продавца, остается под вопросом.
- Случайные комбинации с фенибутом, которые были выявлены фактически, не проверялись в исследованиях.
- Получая аналог или принимая не оригинальный препарат, пациент может получить завышенную или заниженную дозу, что повлияет на эффективность терапии и увеличит риск развития побочных эффектов.
Результаты исследования подчеркивают критическую необходимость контроля, клинической оценки и надежных производственных стандартов для препаратов, применяемых в неврологии.
Как быстро проверить качество препарата?
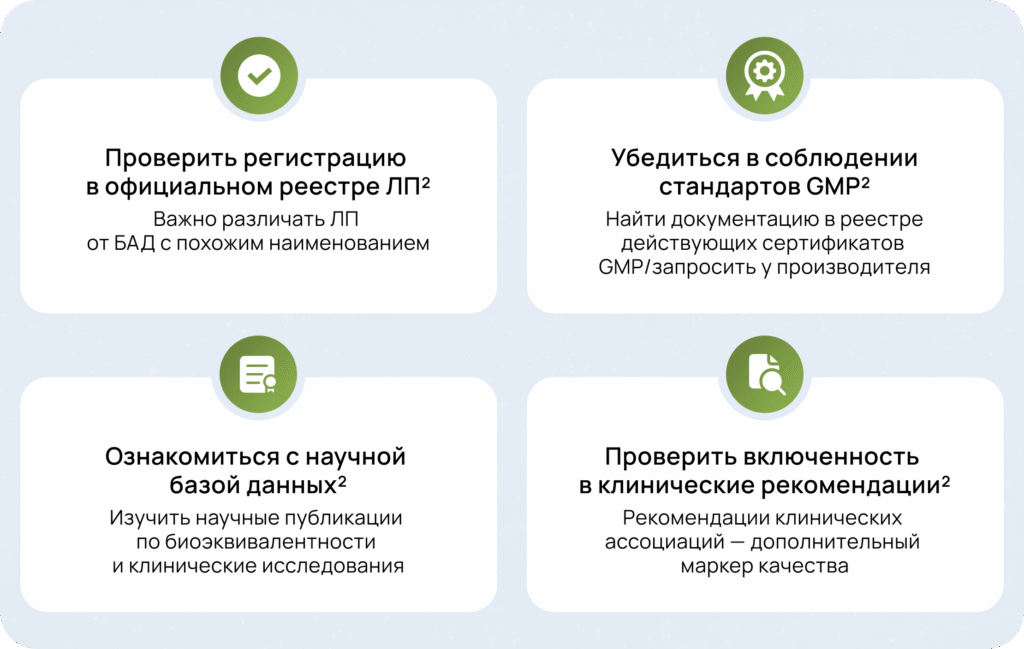

Практические советы при назначении ЛС:
- Отдавать предпочтение оригинальным препаратам с доказанной эффективностью и безопасностью.
- Информировать пациентов о рисках приобретения некачественных препаратов.
Ноофен®
Оригинальный препарат Ноофен® отвечает перечисленным требованиям качества, что повышает эффективность терапии, и обеспечивает предсказуемый клинический результат в неврологической практике.


ЛП — Лекарственный препарат, ЛС — Лекарственное средство, БАД — Биологически активная добавка, GMP — Надлежащая производственная практика.
- Upmanis T, Sevostjanovs E, Zvejniece L, Kazoka H, Kisis V, Pugovics O, Dambrova M. Purchasing “Nootropics” Online: Identification and Quantification of Ingredients in Phenibut-Containing Products. Medicina. 2024; 60(10):1561. https://doi.org/10.3390/medicina601015.
- FDA. Guidances | Drugs [Электронный ресурс] // U.S. Food and Drug Administration. – Режим доступа: https://www.fda.gov/drugs/guidance-compliance-regulatory-information/guidances-drugs (дата обращения: 13.10.2025).
- Инструкция по медицинскому применению препарата Ноофен®, капсулы 500 мг.
- Никитюк В.Г. и соавт. История, преимущества и современная классификация желатиновых капсул. Провизор. 1999; 2:2-34.
- Cole G. Evaluating Development and Production Costs: Tablets Versus Capsules. Pharmacaceutical Technology Europe. 1998; 5:17-26.
- Воробьева, О. В. Эффективность и безопасность препарата ноофен в терапии синдрома хронической усталости у больных с цереброваскулярной недостаточностью / О. В. Воробьева, В. В. Русая // Журнал неврологии и психиатрии им. C.C. Корсакова. – 2017. – Т. 117, № 11. – С. 31-36. – DOI 10.17116/jnevro201711711131-36. – EDN ZXGAJB.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ


Классифицируется по ICHD-3 как вторичная головная боль (раздел 8.2)2.


ЛИГБ часто остается незамеченной, так как симптомы маскируются под другие формы цефалгии1. Именно поэтому важно понимать, почему происходит усугубление течения заболевания и по каким признакам можно своевременно определить данную патологию.
Проблема маскировки и усугубления течения
- ЛИГБ часто скрывается за симптомами основной первичной головной боли1
- Лекарственный абузус — основной фактор трансформации эпизодической цефалгии
- в хроническую1
- Пациенты не могут точно определить причину боли и продолжают принимать привычные препараты1
Базовые критерии по ICHD-3:
Постановка диагноза ЛИГБ требует внимательной оценки множества факторов. Чтобы упростить процесс, приведен пошаговый алгоритм, который помогает быстро и последовательно проанализировать анамнез, исключить альтернативные причины и подтвердить диагноз.
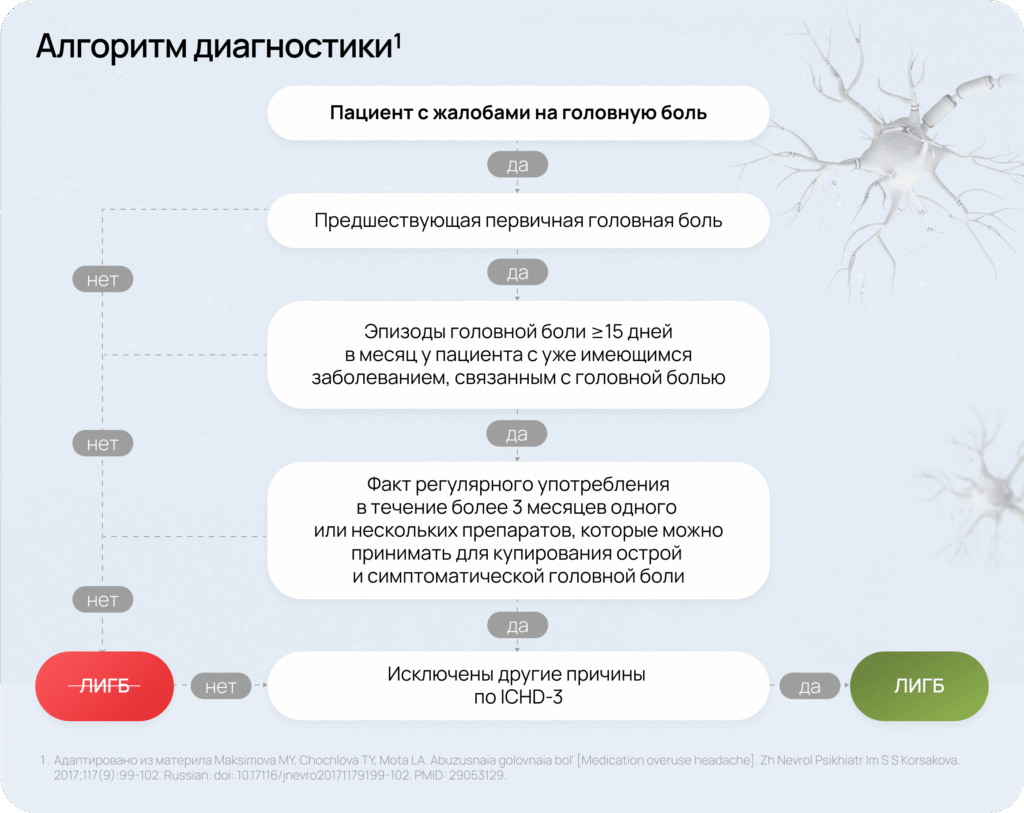
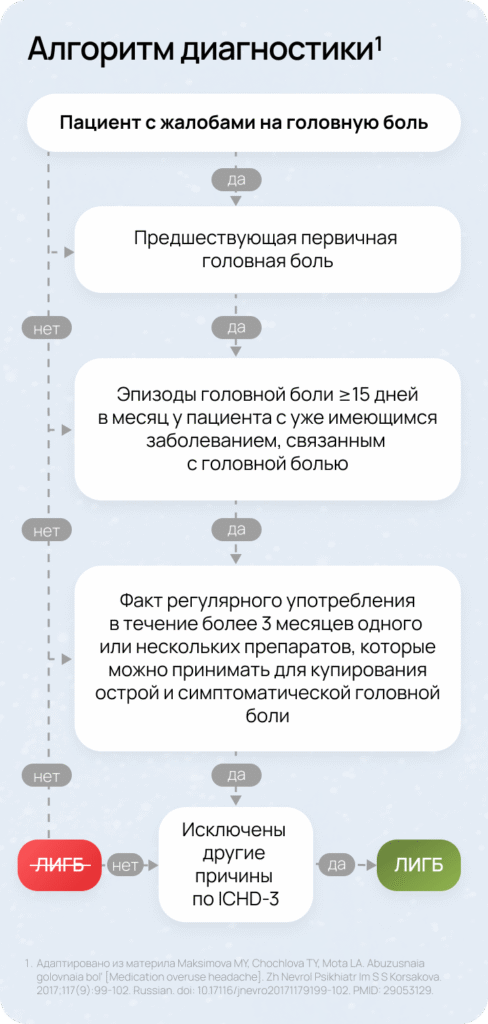
Лечение ЛИГБ должно быть направлено не только на устранение болевого синдрома, но и на предотвращение рецидивов, повышение информированности пациента и восстановление качества жизни4.
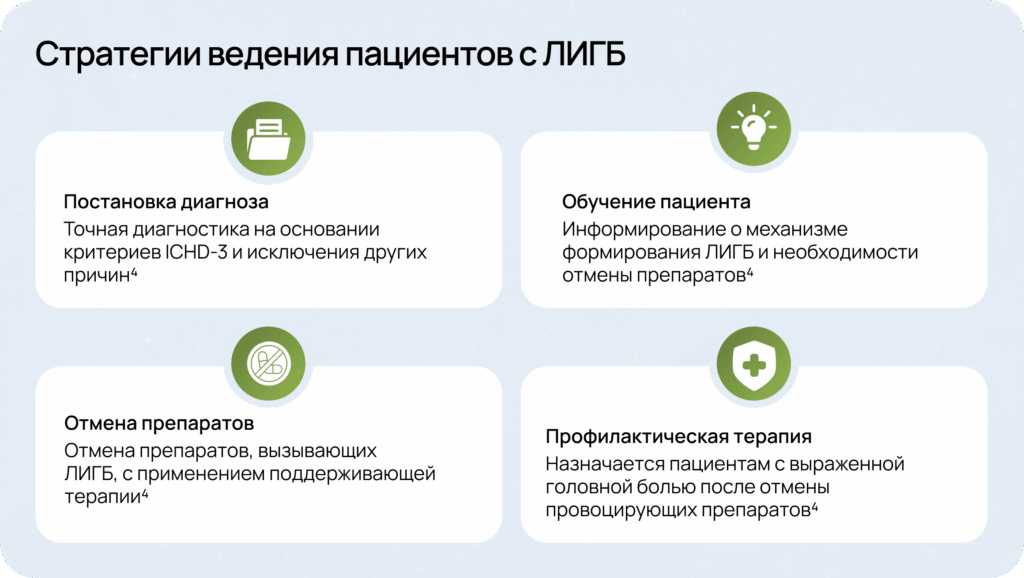
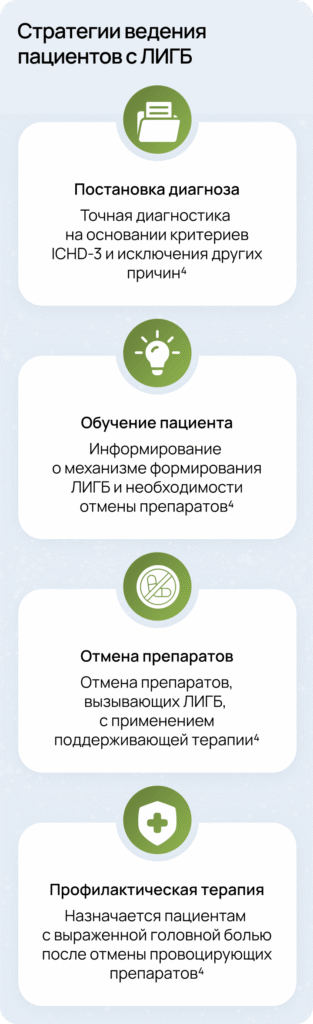
Оптимальным решением для профилактической терапии может стать аминофенилмасляная кислота (например, препарат Ноофен®).
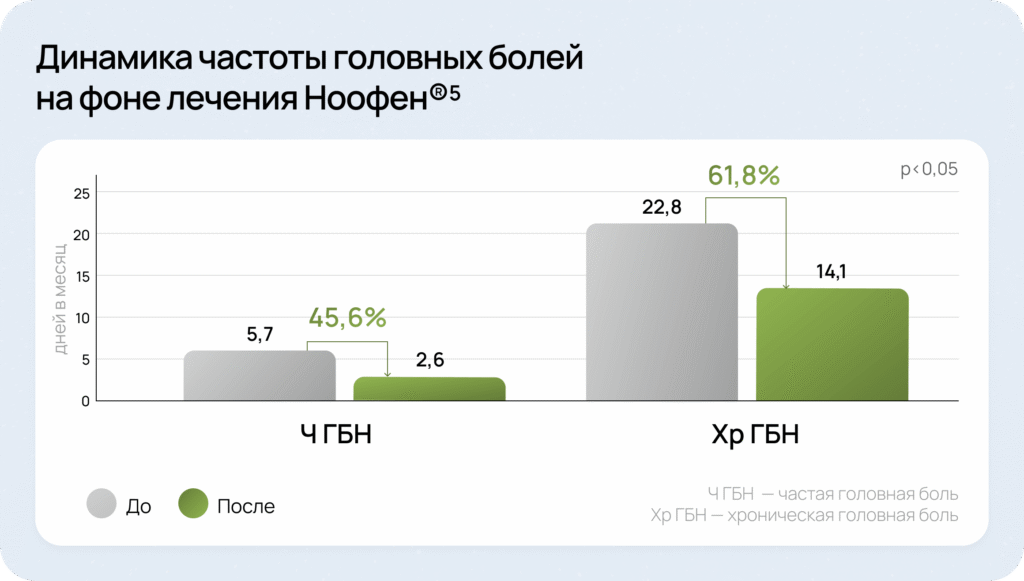
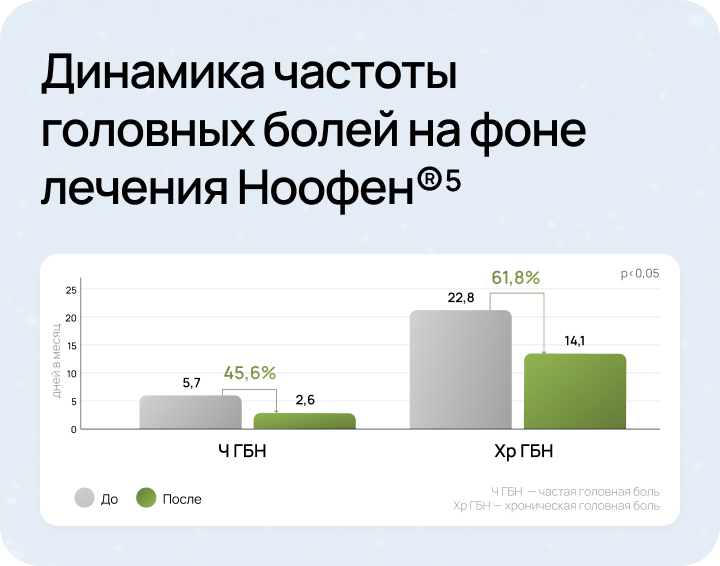
В результате исследования выявлено, что периодичность головной боли уменьшилась на:


Это было достигнуто благодаря:
- Воздействию на ГАМК-рецепторы сосудистой стенки5
- Антиадренергическому действию5
- Нормализации кровотока в артериях Виллизиева круга5




ЛИГБ — лекарственно-индуцированная головная боль. ICHD-3 — Международная классификация головных болей 3-го пересмотра.
- Maksimova MY, Сhochlova TY, Mota LA. Abuzusnaia golovnaia bol’ [Medication overuse headache]. Zh Nevrol Psikhiatr Im S S Korsakova. 2017;117(9):99-102. Russian. doi: 10.17116/jnevro20171179199-102. PMID: 29053129.
- Headache Classification Committee of the International Headache Society (IHS). The International Classification of Headache Disorders, 3rd edition (ICHD-3). Cephalalgia. 2018;38(1):1–211. DOI: 10.1177/0333102417738202. [Электронный ресурс]. URL: https://ichd-3.org/classification-outline (дата обращения: 14.10.2025).
- Medication-overuse headache (MOH) [Электронный ресурс] // International Classification of Headache Disorders, 3rd edition (ICHD-3). URL: https://ichd-3.org/8-headache-attributed-to-a-substance-or-its-withdrawal/8-2-medication-overuse-headache-moh/ (дата обращения: 28.10.2025).
- Kristoffersen, E. S., & Lundqvist, C. (2014). Medication-overuse headache: epidemiology, diagnosis and treatment. Therapeutic advances in drug safety, 5(2), 87–99. https://doi.org/10.1177/2042098614522683.
- Абдуллаев , Р., В. Калашников, О. Щербина, Ф. Куликова, С. . Абрамов, Л. Бабинцева, А. Кириченко, и Г. . Титов. «ВЛИЯНИЕ НООФЕНА НА ЦЕРЕБРАЛЬНУЮ ГЕМОДИНАМИКУ У БОЛЬНЫХ С ГОЛОВНОЙ БОЛЬЮ НАПРЯЖЕНИЯ». Azerbaijan Medical Journal, вып. 3, сентябрь 2022 г., сс. 5-12, doi:10.34921/amj.2022.3.001.
- Дробижев М.Ю. и соавт. Феномен аминофенилмасляной кислоты. РМЖ.2016г., №24. с.1657-1663.
- Садоха, К.А. «Клинический опыт лечения головной боли напряжения.» Медицинские новости. – 2014. – №4.– С. 38–44. Режим доступа: https://cyberleninka.ru/article/n/klinicheskiy-opyt-lecheniya-golovnoy-boli-napryazheniya (дата обращения 14.10.2025).
- Инструкция по медицинскому применению препарата Ноофен®, капсулы 500 мг.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Астенические состояния и расстройства адаптации часто пересекаются в неврологической практике, затрудняя выбор терапии.
МКБ-11, в отличие от МКБ-10, уточнила критерии диагностики и позволила четко разграничить эти состояния, обеспечив более точный и обоснованный терапевтический подход1.
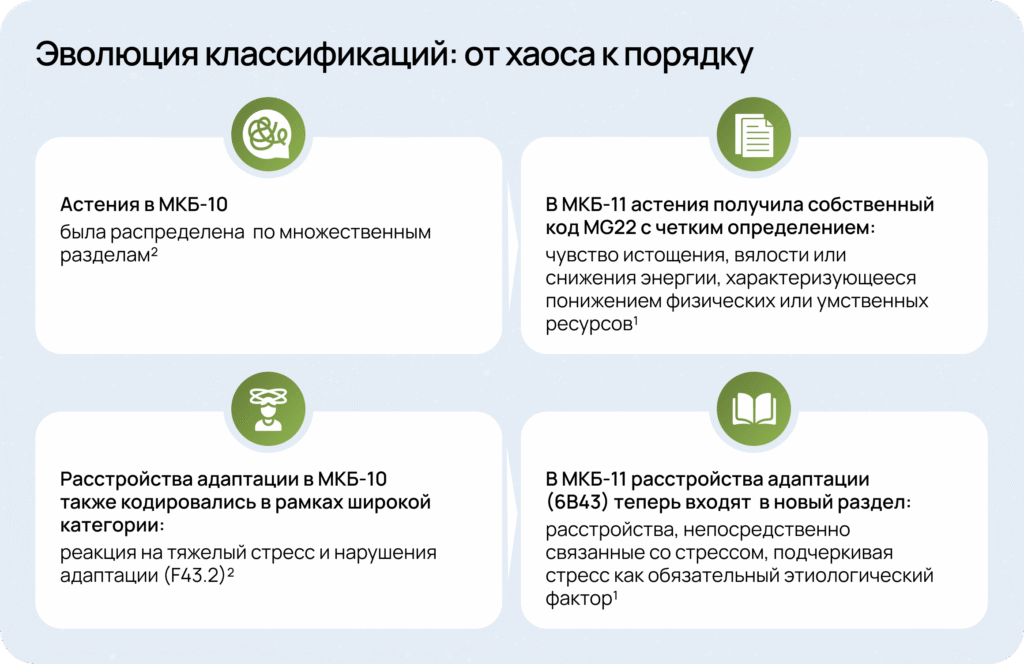

Курс на дифференциальную диагностику
МКБ-11 «уточняет» концепцию динамического реагирования нервной системы, разделяя состояния по временным критериям1,3.
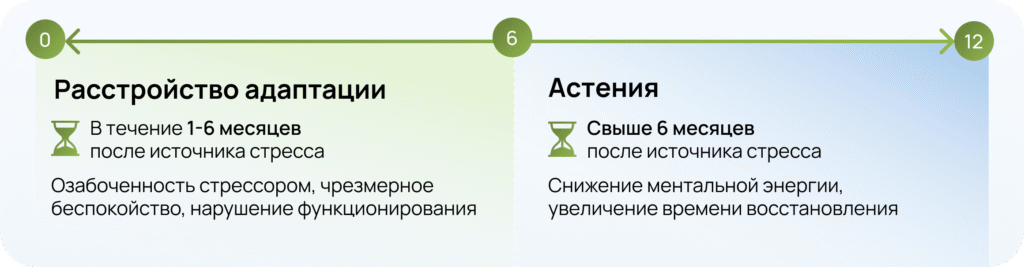

Клиническое значение разграничения
Критерии диагностики
Расстройство адаптации:
- Четкая связь с психосоциальным стрессором4
- Симптомы проявляются в течение 1 месяца после воздействия стресс-фактора4
- Значительное ухудшение социального/ профессионального функционирования4
- Симптомы ослабевают при устранении стрессора4
Астения:
- Характеризуется истощением энергетических ресурсов5
- Может прогрессировать в синдром хронической усталости5
- Часто сочетается с аффективными и когнитивными расстройствами5
- Различают первичную (вызвана стресс-фактором) и вторичную формы (вызвана существующей патологией)5
Подходы к терапии
Расстройство адаптации:
- Когнитивно-поведенческая терапия4
- Краткосрочное вмешательство при адаптационном расстройстве (Brief Adjustment Disorder Intervention)4
- Программа «Навыки адаптации и жизнестойкости» (Skills for Life Adjustment and Resilience)4
Астения:
- Когнитивно-поведенческая терапия6
- Терапия первичной астении включает физические тренинги, психотерапевтические методы и применение различных препаратов6
- Терапия вторичной астении направлена на лечение основного заболевания или купирование сопутствующих симптомов астении6


Результаты исследования:
оценка эффективности и переносимости препарата Ноофен® в терапии синдрома хронической усталости у больных с хронической цереброваскулярной недостаточностью9

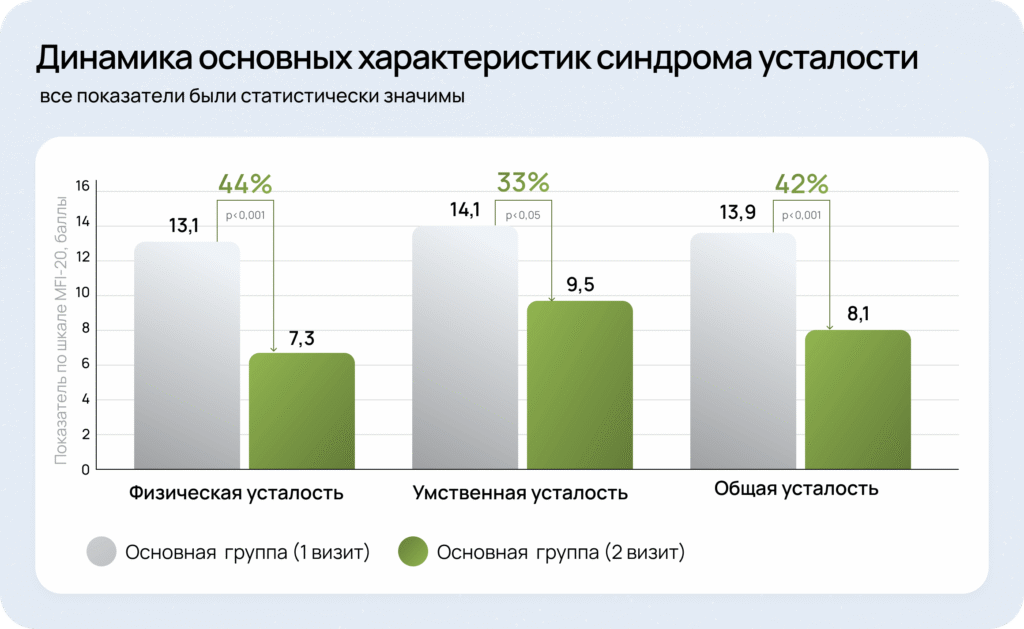


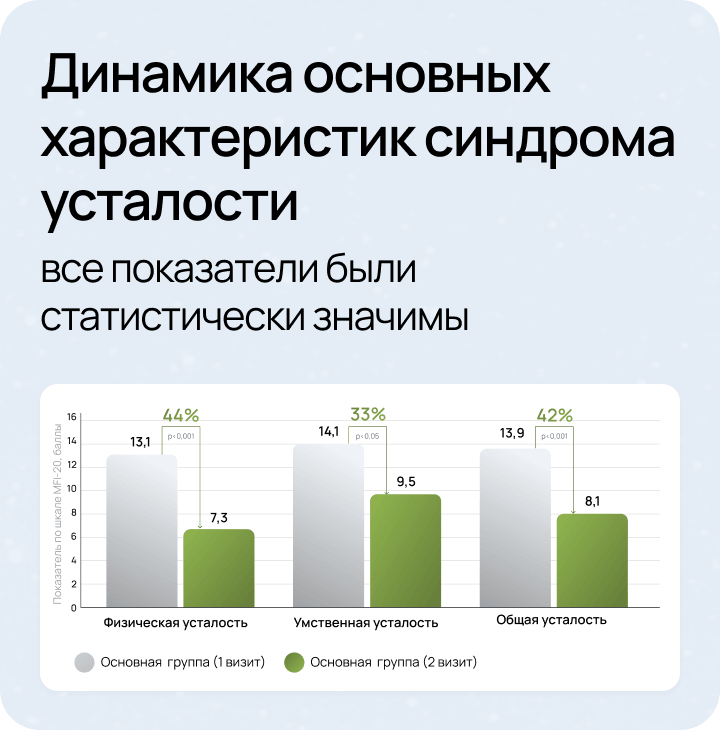

МКБ-10 — Международная классификация болезней 10-го пересмотра, МКБ-11 — Международная классификация болезней 11-го пересмотра, MFI-20 — Шкала оценки усталости (Multidimensional Fatigue Inventory scale)
- ICD-11 for Mortality and Morbidity Statistics. URL: https://icd.who.int/browse/2025-01/mms/en#1109546957 (дата обращения: 30.09.2025).
- ICD-10 Version: 2019. URL: https://icd.who.int/browse10/2019/en (дата обращения: 30.09.2025).
- Lindsäter E, Svärdman F, Wallert J, et al. Exhaustion disorder: scoping review of research on a recently introduced stress-related diagnosis. BJPsych Open. 2022;8(5):e159. doi:10.1192/bjo.2022.559.
- O’Donnell ML, Agathos JA, Metcalf O, Gibson K, Lau W. Adjustment Disorder: Current Developments and Future Directions. Int J Environ Res Public Health. 2019 Jul 16;16(14):2537. doi: 10.3390/ijerph16142537. PMID: 31315203; PMCID: PMC6678970.
- Vasenina EE, Gankina OA, Levin OS. Stress, Asthenia, and Cognitive Disorders. Neurosci Behav Physiol. 2022;52(9):1341-1347. doi: 10.1007/s11055-023-01364-1. Epub 2023 Feb 21. PMID: 36846620; PMCID: PMC9942078.
- Дюкова Г.М. Астенический синдром: проблемы диагностики и терапии. Эффективная фармакотерапия. Неврология и психиатрия. 2012;1:40–45. [Dyukova G.M. Asthenic syndrome: problems of diagnosis and therapy. Effektivnaya farmakoterapiya. Nevrologiya i psikhiatriya. 2012;1:40–45 (in Russ.)].
- Адаптировано из: Дробижев М.Ю. и соавт. Феномен аминофенилмасляной кислоты. РМЖ.2016г., №24. с.1657-1663.
- Астенический синдром: проблемы диагностики и терапии // uMEDp.ru. URL: https://umedp.ru/articles/astenicheskiy_sindrom_problemy_diagnostiki_i_terapii.html (дата обращения: 02.10.2025).
- Воробьева О.В., Русая В.В. Эффективность и безопасность препарата ноофен в терапии синдрома хронической усталости у больных с цереброваскулярной недостаточностью. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017. Т. 117. № 11. C. 31–36. Режим доступа: https://www.mediasphera.ru/issues/zhurnal-nevrologii-i-psikhiatrii-im-s-s-korsakova/2017/11/1199772982017111031?lang=ru (дата обращения 30.09.2025).
- Инструкция по медицинскому применению лекарственного средства Ноофен®, капсулы 500 мг. (дата обращения 30.09.2025).
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Более 30 миллионов человек ежедневно принимают нестероидные противовоспалительные препараты (НПВП)1
Пациенты с хроническими болевыми синдромами воспринимают эту группу препаратов как единственный инструмент контроля боли и качества жизни.

Неправильное купирование острой боли ведет к хронизации процесса5
Согласно исследованию в десятке лидирующих причин, которые влияют на снижение качества жизни, четыре позиции занимают болевые синдромы, а первое место — боль в спине6.
Недостаточное купирование боли в остром периоде, присоединение нейропатического компонента и влияние психосоциальных факторов способствуют хронизации, превращая боль в самостоятельное, труднокурабельное заболевание, требующее особого подхода5.
Хроническая боль как следствие нарушенной нейропластичности
Нейропатическая боль часто имеет хроническое течение и может сохраняться даже после заживления повреждённых тканей, что указывает на то, что механизмы нейропластичности связаны с изменением функции нейронов. Нейропластичность играет ключевую роль в развитии нейропатической боли в ответ на повреждение нейрона7.
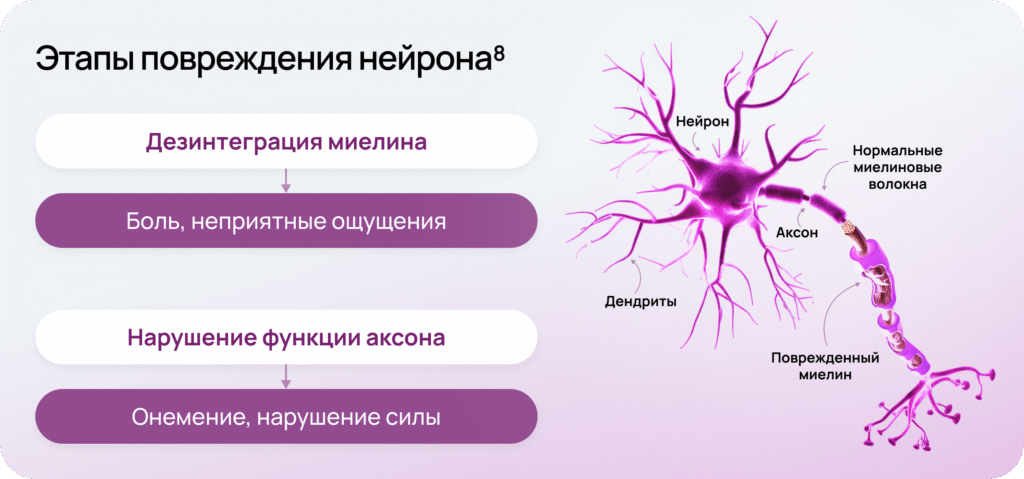

Нейромодуляция: новая цель терапии9
Концепция смещается от «блокирования боли» анальгетическими препаратами к восстановлению нейрональной проводимости и пластичности.

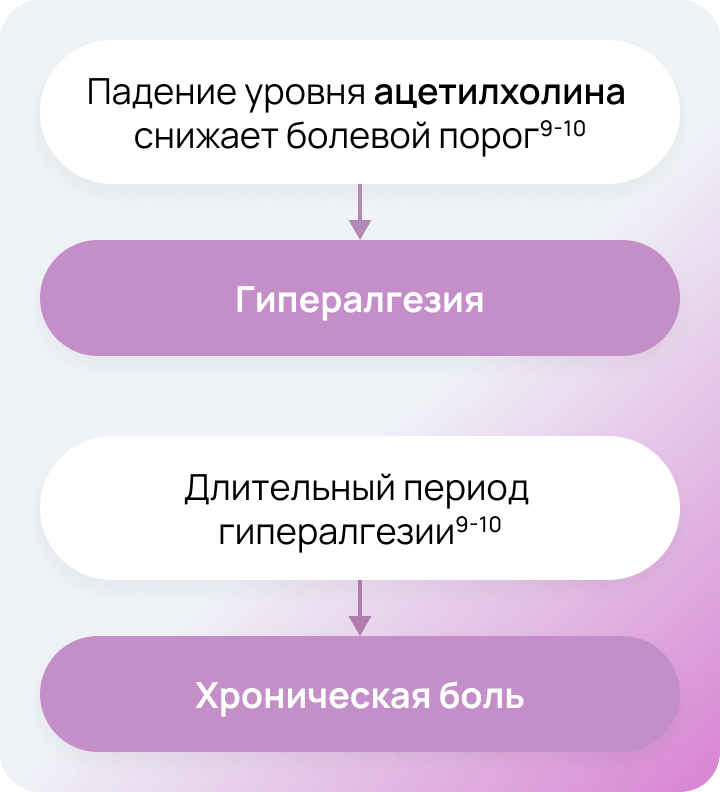
Нормализуем нейронную функцию с помощью регуляции холинергической системы9
Регуляция уровня ацетилхолина с помощью ингибиторов холинэстеразы — современная мера поддержки пациентов с хроническими болями.
Цели:
- усиление холинергической передачи;
- поддержка регенерации нервных волокон;
- улучшение нейросинаптической пластичности.


Нейромидин® (ипидакрин)
Сила восстанавливать нейроны ЦНС и ПНС
В центральной нервной системе
Увеличивает концентрацию ацетилхолина в ЦНС, что приводит к таким эффектам11-14:
- Выделение эндогенных опиоидов
- Высвобождение ГАМК и серотонина
- Снижение уровня норадреналина
- Восстановление нейропластичности
- Повышение уровня BDNF
В комплексе эти факторы проявляют обезболивающее действие в ЦНС11-14.
В периферической нервной системе
Ускоряет функциональное восстановление поражённых корешков и нисходящих нервов15-18:
- Повышает проводимость нервных волокон благодаря увеличению уровня нейромедиатора в синаптической щели
- Восстанавливает мышечную активность, увеличивая силу мышц
- Нормализует чувствительность
Снижает интенсивность болевого синдрома в ПНС15-17.
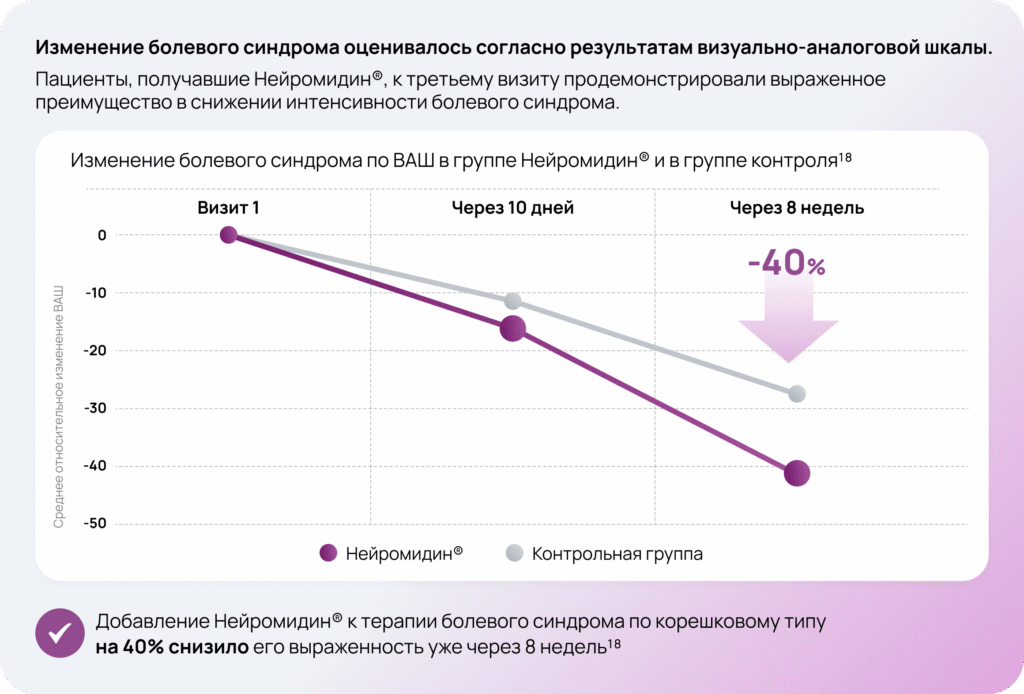
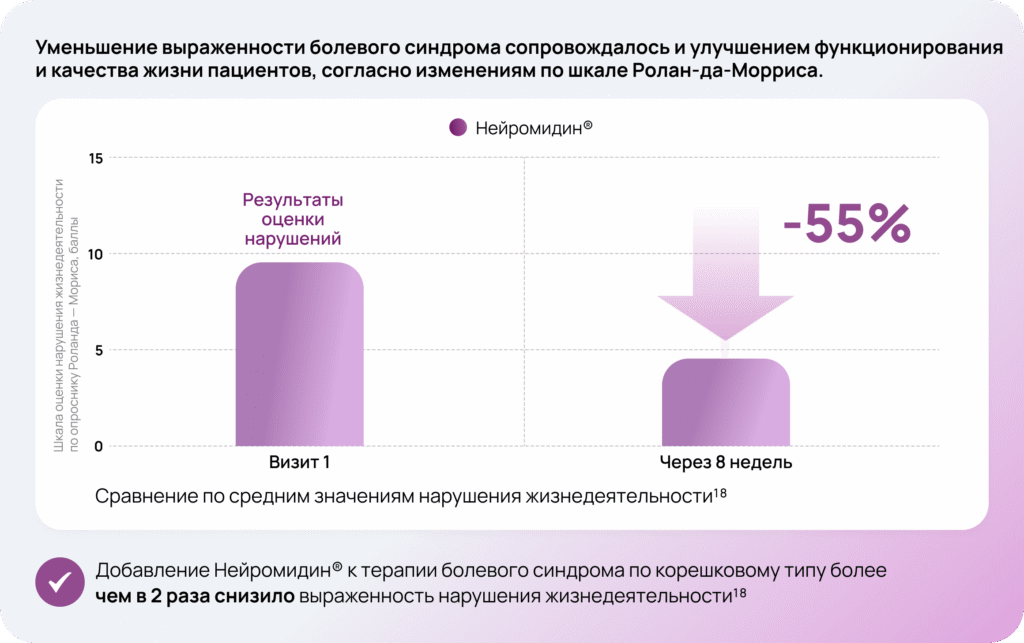
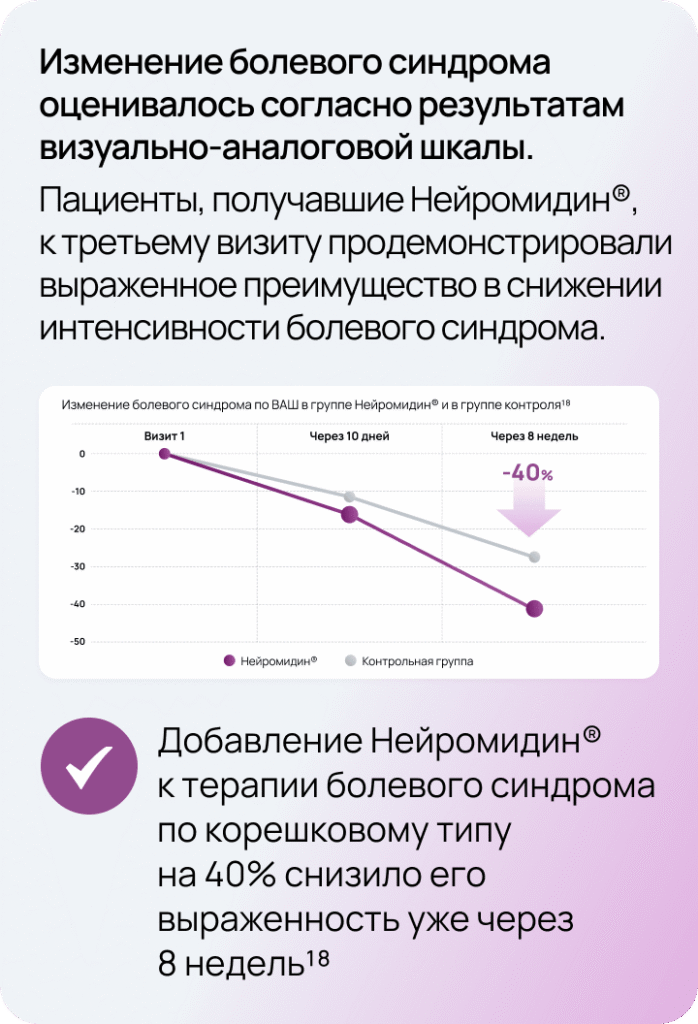
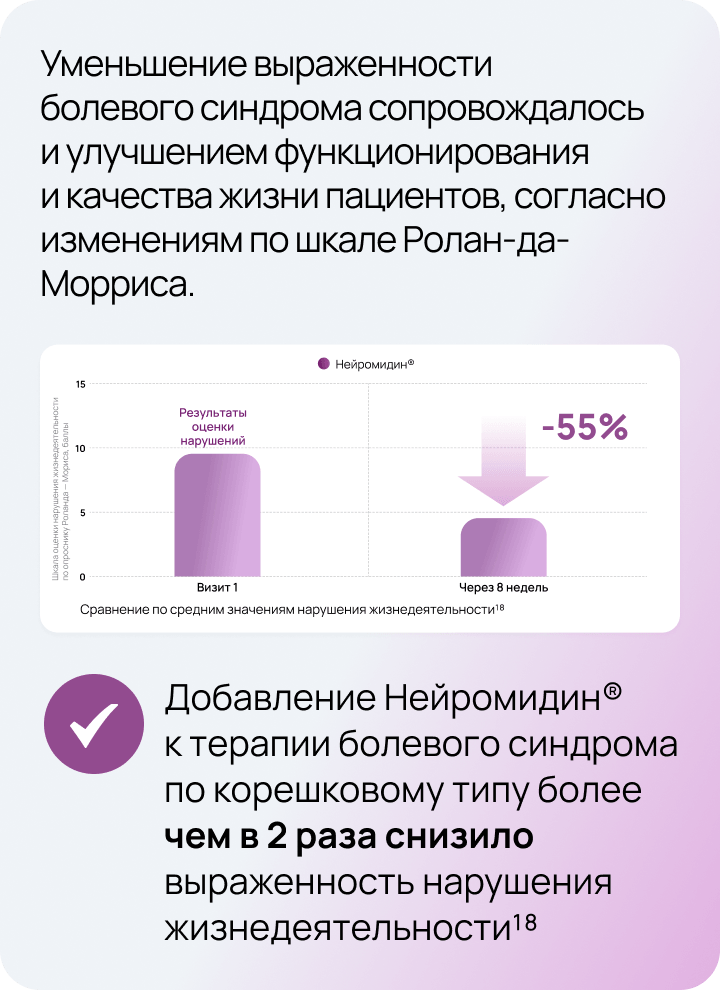
Доказательная база Нейромидин® 18
Дизайн исследования


Ступенчатая терапия
- Инъекционная форма 15 мг/1 мл 1 раз в сутки в/м в течение 10 дней
- Затем таблетированная форма 20 мг 3 таб./сут. до конца 8-й недели общего периода терапии
Режим и дозы терапии подбирались согласно действующей инструкции по медицинскому применению. Эффективность и безопасность терапии в экспериментальной группе определялась как с помощью клинической оценки и опросников, так и нейрофизиологического контроля на электронейромиографии.


НПВП — нестероидные противовоспалительные препараты, ЖКТ — желудочно-кишечный тракт, ЦОГ-2 — циклооксигеназа-2, АХ — ацетилхолин, ЦНС — центральная нервная система, ПНС — периферическая нервная система, ГАМК — гамма-аминомасляная кислота, BDNF — белок мозгового нейротрофического фактора, ВАШ — визуально-аналоговая шкала.
- Sostres C, Gargallo CJ, Lanas A. Nonsteroidal anti-inflammatory drugs and upper and lower gastrointestinal mucosal damage. Arthritis Res Ther. 2013;15 Suppl 3(Suppl 3):S3. doi: 10.1186/ar4175. Epub 2013 Jul 24. PMID: 24267289; PMCID: PMC3890944.
- Scarpignato C, Lanas A, Blandizzi C, Lems WF, Hermann M, Hunt RH; International NSAID Consensus Group. Safe prescribing of non-steroidal anti-inflammatory drugs in patients with osteoarthritis—an expert consensus addressing benefits as well as gastrointestinal and cardiovascular risks. BMC Med. 2015 Mar 19;13:55. doi: 10.1186/s12916-015-0285-8. PMID: 25857826; PMCID: PMC4365808.
- Reimers A, Odin P, Ljung H. Drug-Induced Cognitive Impairment. Drug Saf. 2025 Apr;48(4):339-361. doi: 10.1007/s40264-024-01506-5. Epub 2024 Dec 24. PMID: 39718691; PMCID: PMC11903592.
- Krijthe BP, Heeringa J, Hofman A, Franco OH, Stricker BH. Non-steroidal anti-inflammatory drugs and the risk of atrial fibrillation: a population-based follow-up study. BMJ Open. 2014 Apr 8;4(4):e004059. doi: 10.1136/bmjopen-2013-004059. PMID: 24713211; PMCID: PMC3987714.
- Iakupov ÉZ. Adjuvant therapy of pain syndromes: possibilities of using nucleotides. S.S. Korsakov Journal of Neurology and Psychiatry. 2019;119(10):141‑145. (In Russ.) https://doi.org/10.17116/jnevro2019119101141
- GBD 2015 Disease and Injury Incidence and Prevalence Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015. Lancet. 2016 Oct 8;388(10053):1545-1602. doi: 10.1016/S0140-6736(16)31678-6. Erratum in: Lancet. 2017 Jan 7;389(10064):e1. doi: 10.1016/S0140-6736(16)32606-X. PMID: 27733282; PMCID: PMC5055577.
- Hiraga, Si., Itokazu, T., Nishibe, M. et al. Neuroplasticity related to chronic pain and its modulation by microglia. Inflamm Regener 42, 15 (2022). https://doi.org/10.1186/s41232-022-00199-6
- Общая неврология : учеб. пособие / Д. И. Чиж, Е. В. Петрова, Е. А Кокарева. – Пенза : Изд-во ПГУ, 2019. – 88 с.
- Супонева Н.А., Данилов А.Б., Живолупов С.А. Боль в спине. Концепция назначения антихолинэстеразных препаратов. По материалам Симпозиума «Менеджмент боли в нижней части спины» в рамках XIII Междисциплинарного международного конгресса «Manage Pain» (Управляй болью!), 4–6 ноября 2022 г. (Москва). Manage Pain. 2023; 1:2–8.
- Адаптировано из: Akinci A., Shaker M., Chang M.H. et al. Predictive factors and clinical biomarkers for treatment in patients with chronic pain caused by osteoarthritis with a central sensitisation component. Int J Clin Pract. 2015; 70. doi: 10.1111/ijcp.12749
- Naser P. V. et al. Molecular, Cellular and Circuit Basis of Cholinergic Modulation of Pain. Neuroscience. 2018; 387: 135–148.
- Chen S.P., Kan Y., Zhang J.L. et al. Involvement of hippocampal acetylcholinergic receptors in electroacupuncture analgesia in neuropathic pain rats. Behav Brain Funct. 2016; 12(13).
- Григорова И.А., Тесленко О.А., & Новак А.С. (2018). Влияние Нейромидина® на когнитивные функции и процессы нейропластичности при черепно-мозговой травме. Международный неврологический журнал, (5(99)), 26–33.
- Живолупов С.А., Самарцев И.Н. Центральные механизмы терапевтической эффективности нейромидина в лечении травматических поражений периферической нервной системы. Журнал неврологии и психиатрии им. С.С. Корсакова. 2010; 110(3): 25–30.
- Дамулин И.В., Живолупов С.А. и соавт. Нейромидин в клинической практике. 2-е изд., перераб. и доп. – М.: ООО «Медицинское информационное агентство», 2016. – 60 с. ISBN 978-5-8948-1942-6.
- Самарцев И.Н., Живолупов С.А., Воробьёва М.Н., Паршин М.С., Намждунов Р.З. Оптимизация дифференциальной диагностики и терапии вертеброгенной шейной радикулопатии (исследование ШЕРПА). Журнал неврологии и психиатрии им. С.С. Корсакова. 2020; 120(9): 37–46.
- Боль в спине. Клинический практикум. По материалам Симпозиума «Боль в спине: клинический практикум» в рамках XIX Междисциплинарной конференции с международным участием, посвящённой памяти академика Александра Моисеевича Вейна (8–10 февраля 2023 г., Москва).
- Курушина О.В., Барулин А.Е., Данилов А.Б. Эффективность дифференцированного подхода к лечению боли в спине. Manage Pain. 2024; 1:2–9.
- Инструкция по медицинскому применению лекарственного средства Нейромидин®.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Парез лицевого нерва
Тяжелое состояние, сопровождающееся выраженными психосоциальными последствиями, функциональными нарушениями, эстетическим дефектом и снижением качества жизни1.
Встречаемость паралича Белла в разных популяциях: до 53 человек на 100 000 в год2.


Развитие слабости занимает от нескольких часов до дней. Клиника может нарастать на протяжении нескольких недель, а восстановление занимать месяцы.


Современное представление о патогенетическом механизме согласно руководствам3
Паралич Белла является следствием нарушения периферической функции лицевого нерва из-за воспаления.




Алгоритм диагностики паралича Белла3


Современный комплексный подход к терапии паралича Белла4
Для устранения клинических проявлений необходимо восстановление проводимости лицевого нерва и снятие воспаления3.
Один из препаратов, доказавших эффективность в стимулирующей терапии после завершения острой стадии заболевания, — ипидакрин, ингибитор холинэстеразы4.
Препаратом, стимулирующим восстановление нервно-мышечной передачи, является Нейромидин® (ипидакрин), обратимый ингибитор ацетилхолинэстеразы5.

Эффективность восстановления функции лицевого нерва по данным ЭНМГ
Исследование эффективности было проведено на двух группах пациентов с параличом Белла. Первая группа (n=20) получала базовую терапию (глюкокортикоиды, витамины группы B, пентоксифиллин, глицин, комплекс немедикаментозных методов лечения), а также антихолинэстеразный препарат ипидакрин.
Лечение пациентов контрольной группы (n=15) ограничивалось базовой схемой. Общая длительность периода наблюдения составила 6 месяцев6.
Через 6 месяцев от момента начала терапии и наблюдения в основной группе больных, получавших ипидакрин, восстановление функции ветвей лицевого нерва было более эффективно по сравнению с группой базовой терапии.
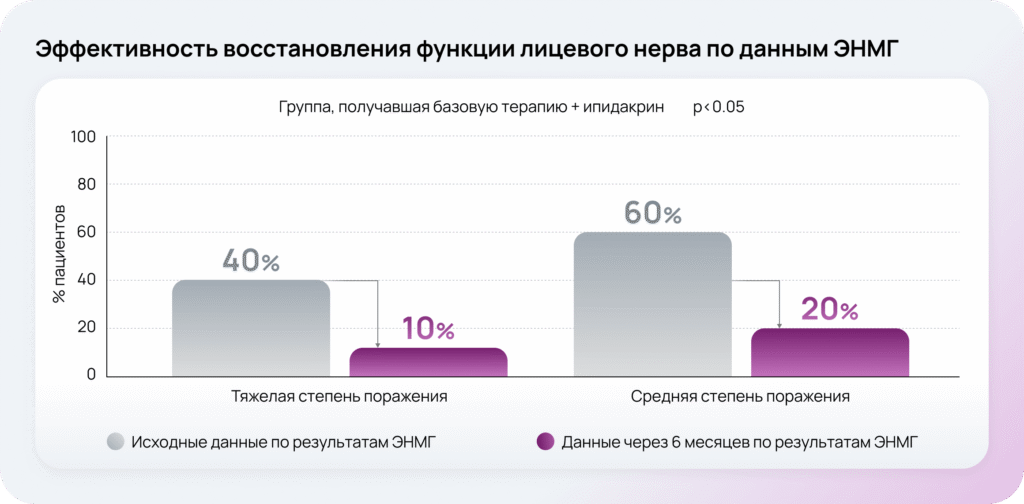
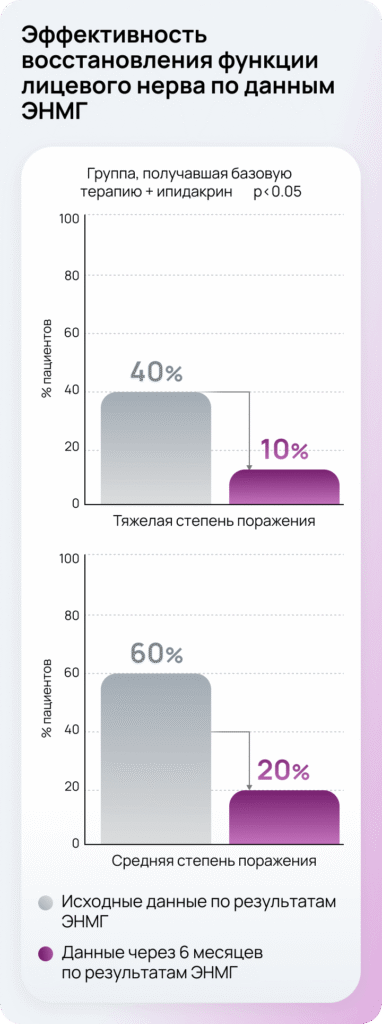
Применение ипидакрина в комплексном лечении пациентов с параличом Белла повышает эффективность восстановления функции лицевого нерва через 6 месяцев без увеличения риска патологических синкинезий (по сравнению с другими АХЭ-препаратами)6.


МРТ — магнитно-резонансная томография, АХЭ — ацетилхолинэстераза, ЭНГМ — электронейромиография
- Shokri, Tom; Saadi, Robert; Schaefer, Eric W.; Lighthall, Jessyka G. . (2020). Trends in the Treatment of Bell’s Palsy. Facial Plastic Surgery, (), s-0040-1713808–. doi:10.1055/s-0040-1713808
- Zhang, W., Xu, L., Luo, T. et al. The etiology of Bell’s palsy: a review. J Neurol 267, 1896–1905 (2020). https://doi.org/10.1007/s00415-019-09282-4
- UpToDate. Bell’s palsy: Pathogenesis, clinical features, and diagnosis in adults. Режим доступа: https://www.uptodate.com/contents/bells-palsy-pathogenesis-clinical-features-and-diagnosis-in-adults (дата обращения: 24.11.2025)
- Клинический протокол “Поражение лицевого нерва” МЗ РК 2013 г.
- Инструкция по медицинскому применению препарата Нейромидин®. РС N014238/01-200122 (дата обращения: 22.12.2024).
- Samartsev I.N., Zhivolupov S.A., Ponomarev V.V., Markova M.N., Magomedov K.R. The efficacy and safety of ipidacrine in patients with idiopathic neuropathy of the facial nerve (PELICAN study). Neurology, Neuropsychiatry, Psychosomatics. 2022; 14(1): 60-68. (In Russ.) https://doi.org/10.14412/2074-2711-2022-1-60-68
- Дамулин И.В., Живолупов С.А. и соавт. Нейромидин в клинической практике. 2-е изд., перераб. и доп. – М.: ООО «Медицинское информационное агентство», 2016. – 60 с. ISBN 978-5-8948-1942-6.
- Живолупов С.А., Самарцев И.Н. Центральные механизмы терапевтической эффективности нейромидина в лечении травматических поражений периферической нервной системы. Журнал неврологии и психиатрии им. С.С. Корсакова. 2010; 110(3): 25–30.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Синдром запястного канала — наиболее распространенная компрессионная мононевропатия, встречающаяся в клинической практике1


Высокая распространённость синдрома запястного канала (СЗК) снижает качество жизни пациентов и увеличивает нагрузку на систему здравоохранения4. Современные методы диагностики и терапии позволяют обеспечить эффективную поддержку таких пациентов.


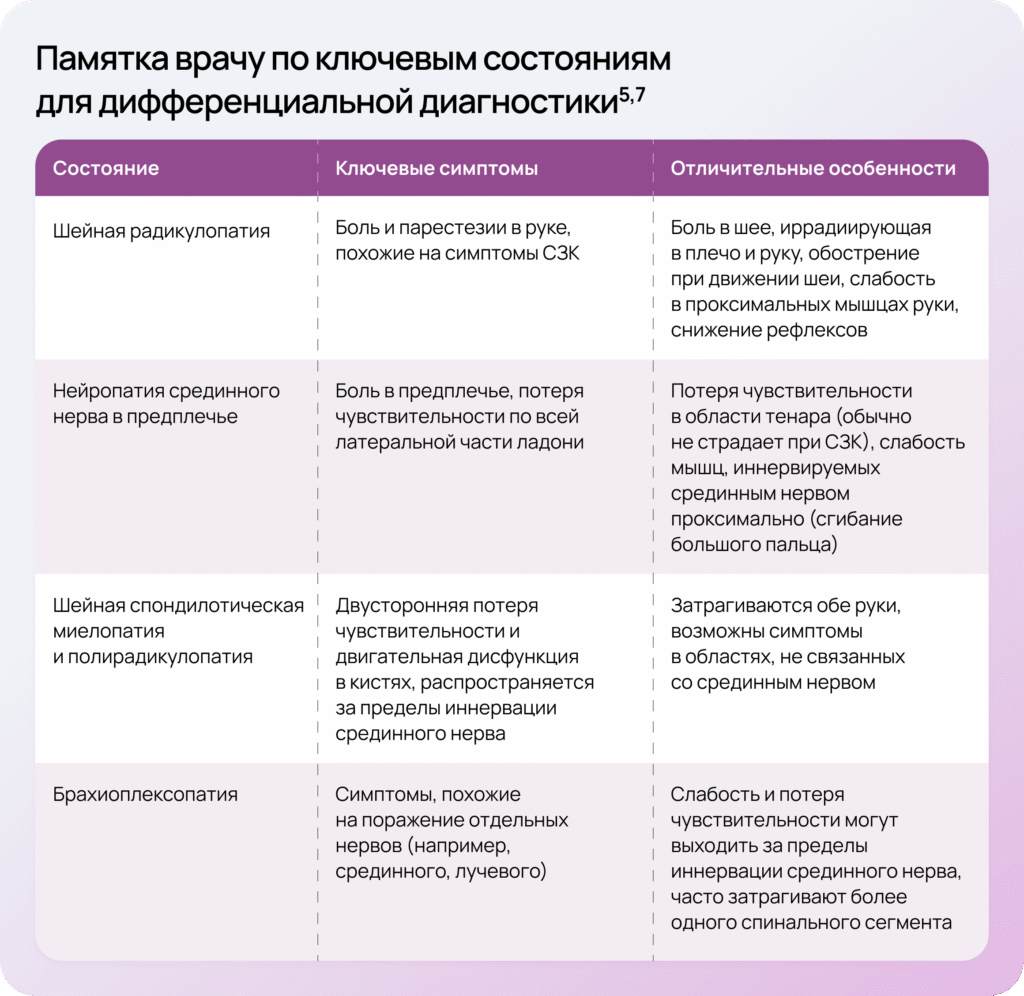
Диагностическая ловушка при дифференциальной диагностике: как не допустить ошибку?
При типичных проявлениях синдрома запястного канала постановка диагноза не затруднительна, однако у части пациентов симптомы могут быть атипичными или напоминать другие заболевания, что требует дифференциальной диагностики5,7.
Заболевания, которые необходимо учитывать при дифференциальной диагностике:
- локтевая невропатия
- плексопатия (поражение плечевого сплетения)
- шейная радикулопатия (C6—C7)
- боковой амиотрофический склероз
- сирингомиелия
- рассеянный склероз
- тендовагиниты
- остеоартроз пястно-фалангового сустава большого пальца

Современные комплексные подходы к терапии направлены на облегчение симптомов4 и повышение качества жизни пациентов

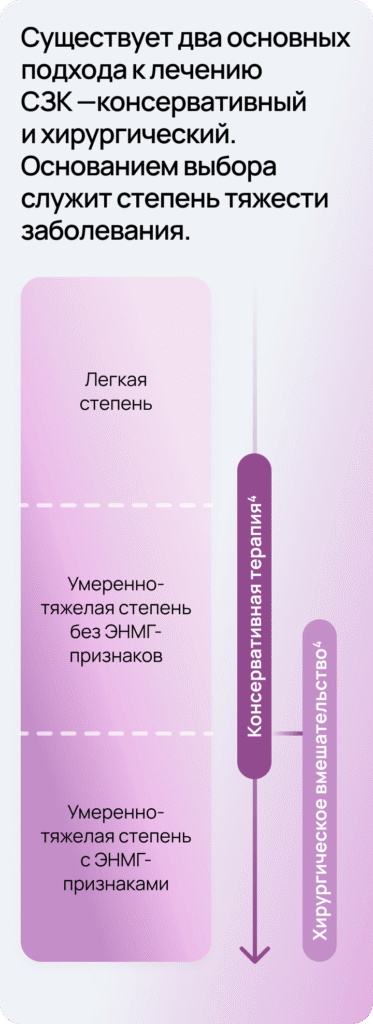
- Консервативная терапия включает иммобилизацию, медикаментозное лечение и физиотерапию. Эти подходы применяются главным образом при легких и умеренных формах СЗК4.
- Хирургическое вмешательство осуществляется при тяжелых формах СЗК и неэффективности консервативных методов4.
Поддержка холинергической регуляции в составе комплексной терапии СЗК
Поиск препаратов, способных положительно влиять на восстановление нервных волокон и улучшать моторные и сенсорные функции, остается актуальной задачей8.

Нейромидин® (Ипидакрин) повышает чувствительность рецепторов постсинаптической мембраны к ацетилхолину, что позволяет эффективнее передавать сигналы от нервов к мышцам9.
Эффективность Нейромидин®: данные Европейского исследования8
Дизайн исследования8
В исследование был включен 51 пациент с СЗК. Диагноз был подтвержден с помощью ЭМГ. Пациенты были разделены на 2 равные по степени тяжести группы:
- 1 группа (25 пациентов): базовая терапия + Нейромидин® 20 мг 2–3 раза в сутки
- 2 группа (26 пациентов): только базовая терапия
В базовую терапию были включены НПВС, сосудистые средства, витамины группы В. Курс терапии длился в среднем 67 дней. Группы оценивались до и после курса терапии с использованием шкал DASH, BCTQ и ВАШ.
Повторная оценка через месяц показала достоверно более выраженное клиническое улучшение в группе, получавшей Нейромидин® 8
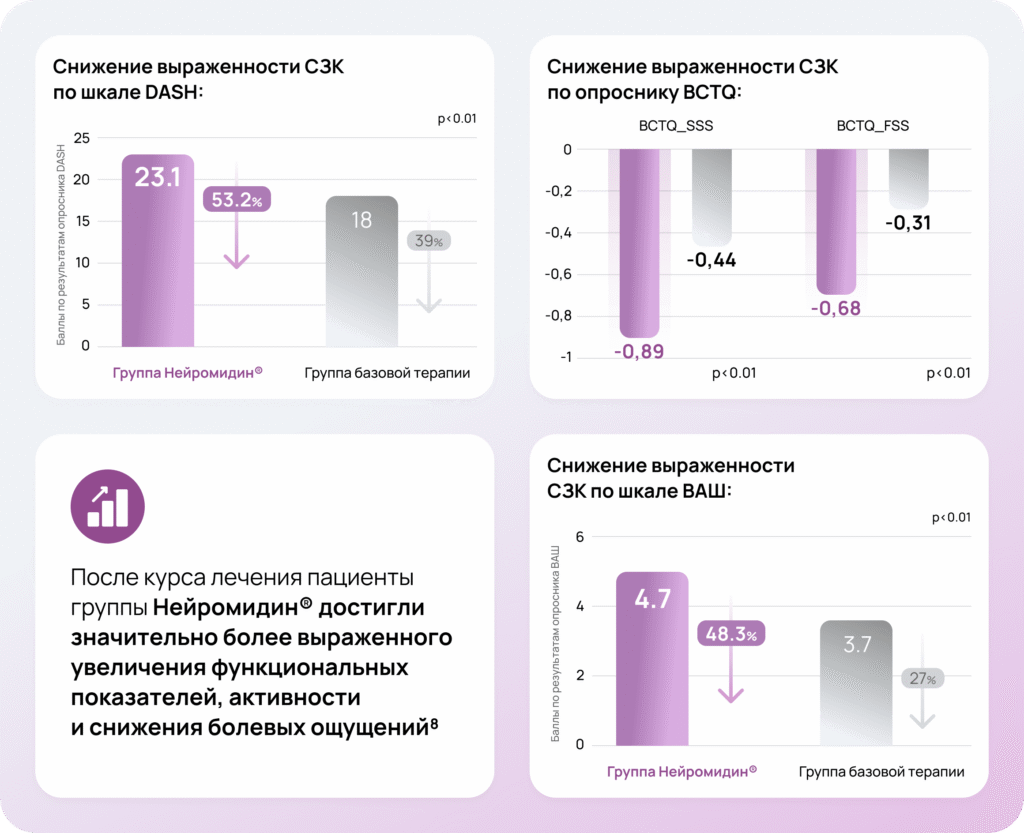
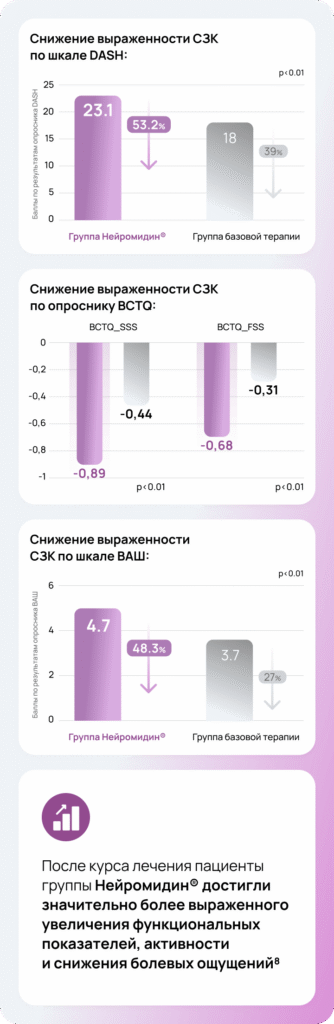


СЗК — синдром запястного канала, ЭНМГ — электронейромиография, ЭМГ — электромиограмма, УЗИ — ультразвуковая диагностика, МРТ — магнитно-резонансная томография, DASH (The disabilities of the arm, shoulder, hand questionnaire) — опросник исходов и неспособности руки и кисти; BCTQ_FSS (Boston carpal Tunnel Syndrome Questionnaire, Function Status Scale) — Бостонский опросник по оценке карпального туннельного синдрома, шкала функционального состояния, BCTQ_SSS (Boston carpal Tunnel Syndrome Questionnaire, Symptom Severity Scale) — Бостонский опросник по оценке карпального туннельного синдрома, шкала тяжести симптомов; ВАШ — визуальная аналоговая шкала, НПВС — нестероидные противовоспалительные средства
- Kothari M.J. Carpal tunnel syndrome: Clinical manifestations and diagnosis. Official reprint from UpToDate®. Available at: https://www.uptodate.com/contents/carpal-tunnel-syndrome-clinical-manifestations-and-diagnosis/print.
- Feng B, Chen K, Zhu X, Ip WY, Andersen LL, Page P, Wang Y. Prevalence and risk factors of self-reported wrist and hand symptoms and clinically confirmed carpal tunnel syndrome among office workers in China: a cross-sectional study. BMC Public Health. 2021 Jan 6;21(1):57. doi: 10.1186/s12889-020-10137-1. PMID: 33407293; PMCID: PMC7789363.
- Gelfman R., Melton L.J. 3rd, Yawn B.P. et al. Long-term trends in carpal tunnel syndrome. Neurology. 2009; 72(1):33–41. DOI: 10.1212/01.wnl.0000338533.88960.b9. PMID: 19122028; PMCID: PMC2633642.
- Malakootian M, Soveizi M, Gholipour A, Oveisee M. Pathophysiology, Diagnosis, Treatment, and Genetics of Carpal Tunnel Syndrome: A Review. Cell Mol Neurobiol. 2023 Jul;43(5):1817-1831. doi: 10.1007/s10571-022-01297-2. Epub 2022 Oct 10. PMID: 36217059; PMCID: PMC11412174.
- Bland JD. Carpal tunnel syndrome. BMJ. 2007 Aug 18;335(7615):343-6. doi: 10.1136/bmj.39282.623553.AD. PMID: 17703044; PMCID: PMC1949464.
- Graham B, Peljovich AE, Afra R, Cho MS, Gray R, Stephenson J, Gurman A, MacDermid J, Mlady G, Patel AT, Rempel D, Rozental TD, Salajegheh MK, Keith MW, Jevsevar DS, Shea KG, Bozic KJ, Adams J, Evans JM, Lubahn J, Ray WZ, Spinner R, Thomson G, Shaffer WO, Cummins DS, Murray JN, Mohiuddin M, Mullen K, Shores P, Woznica A, Linskey E, Martinez Y, Sevarino K. The American Academy of Orthopaedic Surgeons Evidence-Based Clinical Practice Guideline on: Management of Carpal Tunnel Syndrome. J Bone Joint Surg Am. 2016 Oct 19;98(20):1750-1754. doi: 10.2106/JBJS.16.00719. PMID: 27869627.
- Preston DC, Shapiro BE. Median neuropathy at the wrist. In: Electromyography and Neuromuscular Disorders: Clinical-Electrophysiologic-Ultrasound Correlations, 4th ed, Elsevier, Philadelphia 2020. p.323.
- Rubens O, Bērziņa S, Rozenbaha A, Dansone G, Troshina Y. Exploring the Non-Invasive Approaches to Carpal Tunnel Syndrome in Routine Clinical Practice: A Focus on the Role of Acetylcholinesterase Inhibitors. Medicina (Kaunas). 2024 Jul 27;60(8):1219. doi: 10.3390/medicina60081219. PMID: 39202499; PMCID: PMC11356180.
- Волосовець А.О. Сучасний підхід до корекції неврологічного дефіциту внаслідок карпального тунельного синдрому. Здоров’я України. 2024; 2.
- Инструкция по медицинскому применению препарата Нейромидин®. РС N014238/01-200122 (дата обращения: 27.10.2025).
- Живолупов С.А., Самарцев И.Н. Центральные механизмы терапевтической эффективности нейромидина в лечении травматических поражений периферической нервной системы. Журнал неврологии и психиатрии им. С.С. Корсакова. 2010; 110(3): 25–30.
- Дамулин И.В., Живолупов С.А. и соавт. Нейромидин в клинической практике. 2-е изд., перераб. и доп. – М.: ООО «Медицинское информационное агентство», 2016. – 60 с. ISBN 978-5-8948-1942-6.
- Самарцев И.Н., Живолупов С.А., Воробьева М.Н., Паршин М.С., Нажмудинов Р.З. Оптимизация дифференциальной диагностики и терапии вертеброгенной шейной радикулопатии (исследование ШЕРПА). Журнал неврологии и психиатрии им. С.С. Корсакова. 2020; 120(9): 37–46.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Инсульт — вторая по частоте причина смертности в мире1
За последние 30 лет возросли1:


Когда холин перестает быть полезным: обратная сторона «добавок для мозга»
Экзогенный холин назначается в виде добавок, например, L-альфа-глицерилфосфорилхолина, для профилактики деменции и дисфункции холинергической системы.
Попадая в организм, холин при участии кишечной микрофлоры синтезируется в триметиламиноксид (ТМАО).
В чем же опасность метаболита ТМАО2?
- Усиливает образование пенистых клеток и рост атеросклеротических бляшек.
- Является одной из причин эндотелиальной дисфункции — воспаления эндотелия.
- Повышает агрегацию тромбоцитов и риск ишемического инсульта.
L-альфа-глицерилфосфорилхолин (холина альфосцерат): что говорит наука о приеме экзогенного холина3
Результаты 10-летнего когортного исследования с участием более 12 млн. человек показали3:
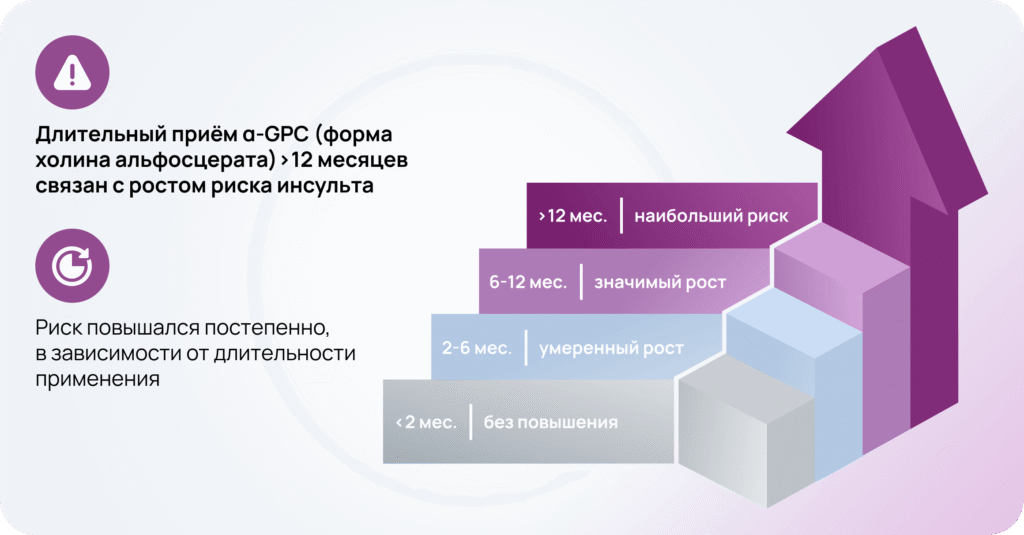

Назначение донаторов холина пациентам с сосудистым риском требует индивидуального подхода с учётом метаболических особенностей и состава кишечной микробиоты; неконтролируемое использование БАДов и препаратов с высокими дозами холина следует избегать.
Какую безопасную поддержку холинергической регуляции подобрать для пациентов, перенесших инсульт?
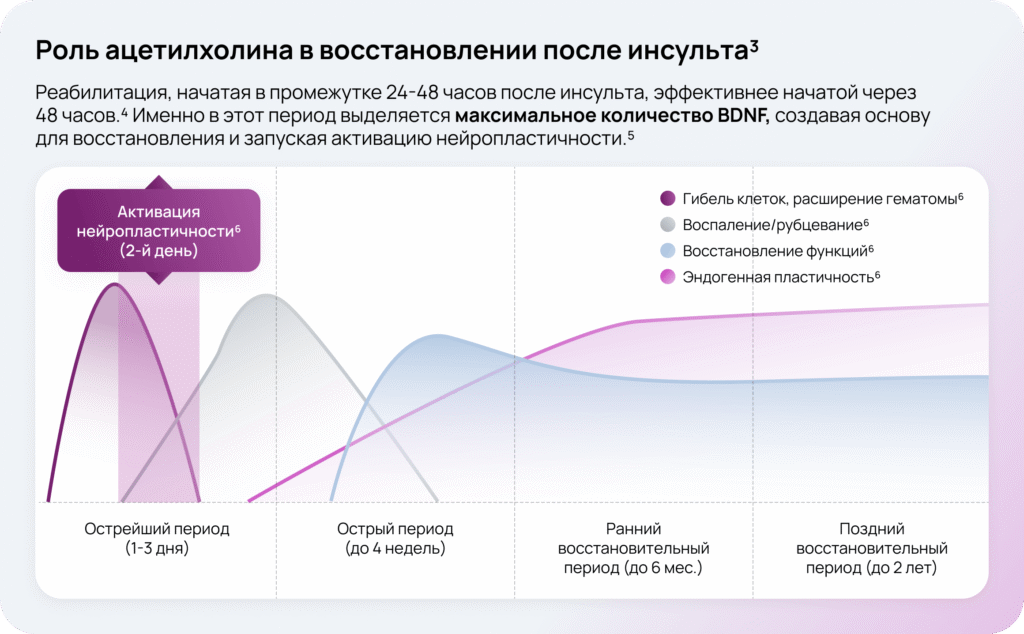
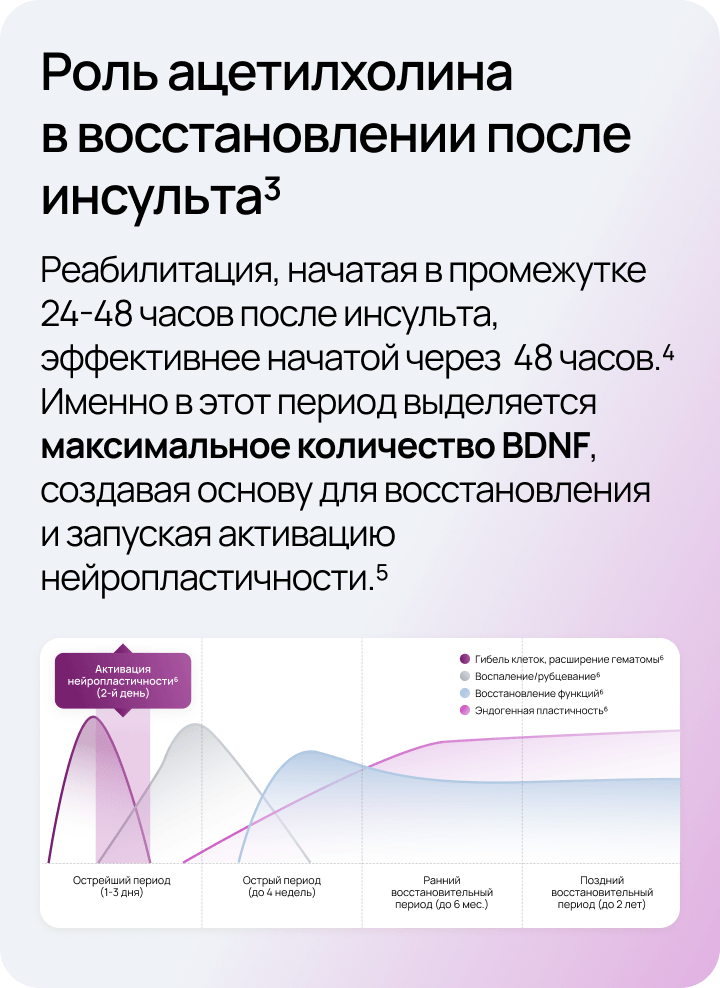
Ацетилхолин через мускариновые и никотиновые рецепторы, особенно α7-nAChR, активирует внутриклеточные сигнальные каскады, которые запускают транскрипцию гена BDNF5.
Нейромидин® (ипидакрин), обратимый ингибитор ацетилхолинэстеразы, повышает концентрацию эндогенного ацетилхолина в синапсах, блокируя его распад 11.
Актуальная стратегия восстановления функций после инсульта


В рандомизированном исследовании, включавшем пациентов с ишемическим инсультом каротидного бассейна, добавление Нейромидин® к стандартной терапии способствовало более выраженному восстановлению неврологических функций по сравнению с контрольной группой. Препарат хорошо переносился, побочных эффектов не зафиксировано9.
Общая оценка эффективности лечения
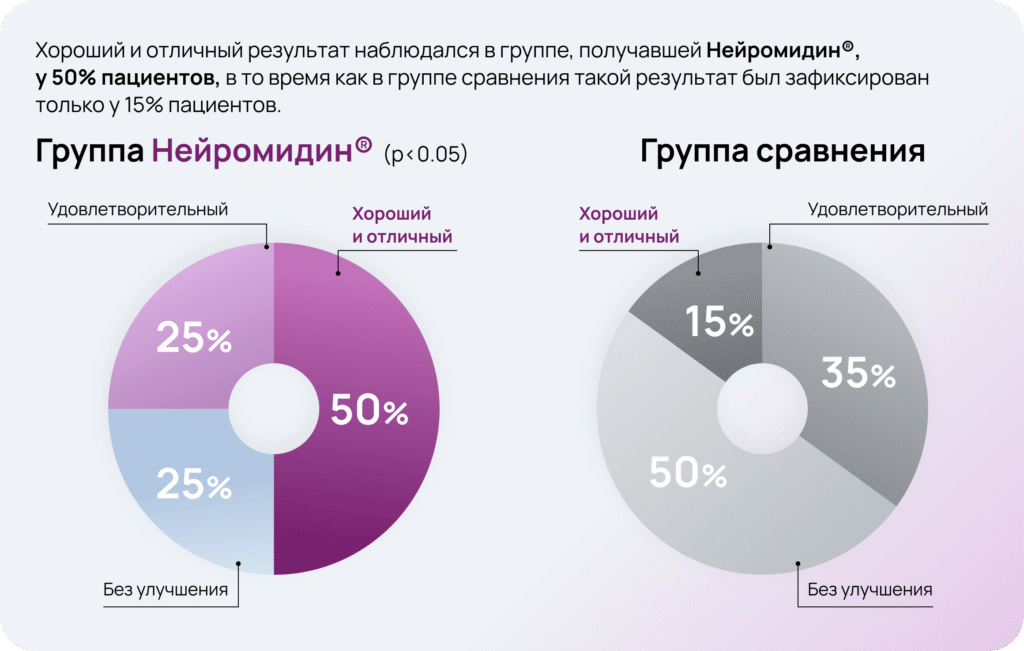
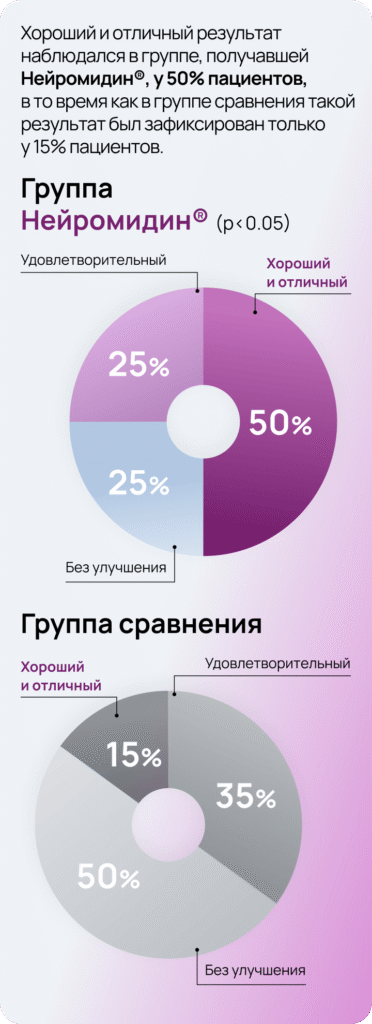
При лечении препаратом Нейромидин® отмечалось постепенное уменьшение выраженности неврологической симптоматики, и к 80-м суткам после инсульта неврологический статус по СШИ улучшился в среднем на 22%. Тяжесть инсульта стала соответствовать лёгкой степени.
При оценке динамики пациентов, получавших только базисную терапию, статистически значимых различий между исходным уровнем и спустя 80 дней после начала терапии не выявлено.
Схема назначения препарата Нейромидин® в остром периоде инсульта10,11
- В течение 14 дней: в/м раствор 15 мг/мл по 1 мл 2 раза в сутки.
- Затем продолжают терапию, перейдя на таблетированную форму: 40 мг в сутки (по 1 таблетке 2 раза в сутки) в течение 45–90 дней.
В острый период инсульта Нейромидин® включают в базовую терапию только после стабилизации состояния пациента.
ТМАО — триметиламиноксид, ТМА — триметиламин, α-GPC — L-альфа-глицерилфосфорилхолин, БАД — биологически активная добавка, BDNF (brain-derived neurotrophic factor) — белок мозгового нейротрофического фактора, ЦНС — центральная нервная система, ПНС — периферическая нервная система, СШИ — скандинавская шкала инсульта.
- GBD 2019 Stroke Collaborators. «Global, regional, and national burden of stroke and its risk factors, 1990–2019: a systematic analysis for the Global Burden of Disease Study 2019.» Lancet Neurol., vol. 20, 2021, pp. 795–820. Published Online September 3, 2021. doi: 10.1016/S1474-4422(21)00252-0.
- Zhu Y. et al. Gut microbiota in atherosclerosis: focus on trimethylamine N-oxide. APMIS, 2020; 128(5):353-366. DOI: 10.1111/apm.13038 JAMA Netw Open Published Online: November 24, 2021;4;(11):e2136008. doi:10.1001/jamanetworkopen.2021.36008.
- Lee G, Choi S, Chang J, Choi D, Son JS, Kim K, Kim SM, Jeong S, Park SM. Association of L-α Glycerylphosphorylcholine With Subsequent Stroke Risk After 10 Years. JAMA Netw Open. 2021 Nov 1;4(11):e2136008. doi: 10.1001/jamanetworkopen.2021.36008. PMID: 34817582; PMCID: PMC8613599.
- Otokita S. et al. Impact of rehabilitation start time on functional outcomes after stroke. Journal of Rehabilitation Medicine. 2021; 53(1): jrm00145. doi: 10.2340/16501977-2775
- Liu Yi et al. Early Rehabilitation after Acute Stroke: The Golden Recovery Period. Acta Neurologica Taiwanica, 2022.
- Адаптировано по материалам: Bernhardt J., Hayward K.S., Kwakkel G. et al. Agreed definitions and a shared vision for new standards in stroke recovery research: The Stroke Recovery and Rehabilitation Roundtable Taskforce. International Journal of Stroke. 2017; 12(5): 444–450. doi: 10.1177/1747493017711816
- Fernandes C.C. et al. Postsynaptic action of brain-derived neurotrophic factor attenuates alpha7 nicotinic acetylcholine receptor-mediated responses in hippocampal interneurons. Journal of Neuroscience. 2008; 28(21):5611–8. doi: 10.1523/JNEUROSCI.5378-07.2008 PMID: 18495895; PMCID: PMC6670615.
- Bathina S., Undurti N.D. Brain-derived neurotrophic factor and its clinical implications. Archives of Medical Science. 2015; 11(6):1164–78. doi: 10.5114/aoms.2015.56342
- Maximova M.Yu. et al. Neyromidin in ischemic stroke. Journal of Neurology and Psychiatry. 2013; 3.
- Дамулин И. В. с соавт. Нейромидин® в клинической практике. 2-е изд., перераб. и доп. — М.: ООО «Медицинское информационное агентство», 2016. — 60 стр. ISBN 978-5-8948-1942-6.
- Инструкция по медицинскому применению лекарственного средства Нейромидин®.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Сигнал покоя: ацетилхолин в действии
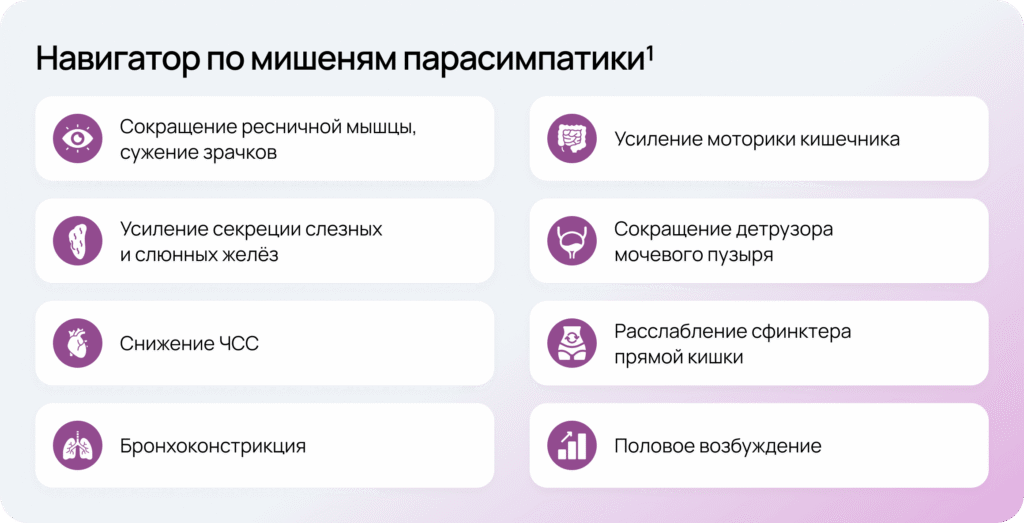
Ацетилхолин — основной нейротрансмиттер парасимпатической системы. Сигнал проходит через никотиновые рецепторы ганглиев, а затем через мускариновые рецепторы периферических органов, регулируя выраженность автономных функций1.
При ослаблении холинергической передачи формируется спектр проявлений дизавтономии — прежде всего ортостатические жалобы, желудочно-кишечные симптомы, урологические нарушения, а также проблемы секреции, нередко сочетающиеся с нарушениями зрачковых реакций и терморегуляции.

Свежий взгляд на диагностику нарушений2: COMPASS-31
Уникальным компонентом скрининга нарушений является Composite Autonomic Symptom Score — 31 (COMPASS-31)3, он помогает эффективно оценить наличие и локализацию нарушения в работе систем органов, а последующее целенаправленное обследование уточняет дисфункцию и ее степень.


Практическое применение: оптимизируем подход к диагностике
- COMPASS-31 — удобный инструмент оценки вегетативных симптомов, позволяющий определить степень тяжести дизавтономии и локализацию
- Опросник оптимизирует клинический поиск и динамическую оценку состояния пациентов с вегетативной недостаточностью
Ацетилхолин: активатор холинергического пути
Ацетилхолин участвует в передаче импульса в нервной системе, а также играет ключевую роль в регуляции работы систем органов4. Даже незначительные нарушения его уровня могут способствовать развитию хронических патологических процессов4.
Низкий уровень холинэстеразы один из признаков суперэйджеров5
Суперэйджеры — люди старше 80 лет, чьи когнитивные способности на среднестатистическом уровне людей среднего возраста.

Нейромидин® (ипидакрин)
Обратимый ингибитор ацетилхолинэстеразы, усиливает холинергеческую передачу4,8 в парасимпатической системе.
Увеличение концентрации ключевого нейротрансмиттера ацетилхолина обеспечивает:
- Восстановление когнитивного резерва6
- Восстановление нервно-мышечной передачи
- Регенерацию поврежденных нервных волокон7,8


COMPASS-31 — Composite Autonomic Symptom Score — 31, комплексная шкала оценки симптомов 6 автономных доменов; ЦНС — центральная нервная система; ПНС — периферическая нервная система, ЧСС — частота сердечных сокращений.
- LeBouef T, Yaker Z, Whited L. Physiology, Autonomic Nervous System. [Updated 2023 May 1]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK538516/
- Sánchez-Manso JC, Gujarathi R, Varacallo MA. Autonomic Dysfunction. [Updated 2023 Aug 4]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK430888/
- Sletten, D. M., Suarez, G. A., & Low, P. A. (2012b). COMPASS 31: A Refined and Abbreviated Composite Autonomic Symptom Score. Mayo Clinic Proceedings, 87(12), 1196–1201. Accessed: https://www.hattrevaluationtools.eu/compass-31/
- Mohan, V., Kaushik, D., & Arora, K. (2023). Role of Acetylcholine in Chronic Diseases. IntechOpen. doi: 10.5772/intechopen.110663
- Janeczek M, Gefen T, Samimi M, Kim G, Weintraub S, Bigio E, Rogalski E, Mesulam MM, Geula C. Variations in Acetylcholinesterase Activity within Human Cortical Pyramidal Neurons Across Age and Cognitive Trajectories. Cereb Cortex. 2018 Apr 1;28(4):1329-1337. doi: 10.1093/cercor/bhx047. PMID: 28334147; PMCID: PMC6059146.
- Дамулин И.В. с соавт. Нейромидин в клинической практике. 2-с изд., перераб. и доп. — М.: ООО «Медицинское информационное агентство». 2016. – 60 с. ISDB 978-5-8948-1942-6.
- Живолупов C.А., Самарцев И.Н. Центральные механизмы терапевтической эффективности нейромидина в лечении травматических поражений периферической нервной системы. Журнал неврологии и психиатрии им. С.С. Корсакова. 2010; 110(3): 25–30.
- Самарцев И.Н., Живолупов С.А., Воробьева М.Н., Паршин М.С., Нажмудинов Р.З. Оптимизация дифференциальной диагностики и терапии вертеброгенной шейной радикулопатии (исследование ШЕРПА). Журнал неврологии и психиатрии им. С.С. Корсакова. 2020; 120(9):37-46.
- Инструкция по медицинскому применению лекарственного средства Нейромидин®, таблетки 20 г.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
