Влияние различных местных АБП на количество бактерий на слизистой оболочке глотки и миндалин у пациентов с острым фарингитом
Айгарс Рейнис1, Гуна Дансоне2, Лига Балоде2,* , Сандра Гинтере3, Андрейс Толстикс4, Катрина Вербовенко5, Олегс Зашибаевс4 и Тайра Сафина4
- Кафедра биологии и микробиологии, Рижский университет имени Страдыня (RSU), ул. Дзирциема, 16, LV-1007 Рига, Латвия
- Отделение медицинских и клинических исследований, АО «Олфа», ул. Рупницу, 5, LV-2114 Олайне, Латвия
- Амбулаторная клиника, Рижский университет имени Страдыня (RSU), ул. Дзирциема, 16, LV-1007 Рига, Латвия
- Факультет резидентуры, Рижский университет имени Страдыня (RSU), ул. Дзирциема, 16, LV-1007 Рига, Латвия
- Медицинский факультет, Рижский университет имени Страдыня (RSU), ул. Дзирциема, 16, LV-1007 Рига, Латвия
Резюме: Актуальность и задачи исследования: Инфекции верхних дыхательных путей — одна из самых распространённых причин обращения за медицинской помощью в амбулаторных условиях. Острый фарингит обычно вызывается вирусами и проходит самостоятельно, но в 30% случаев может развиться вторичная бактериальная инфекция, которая требует антибактериального лечения. В условиях растущей устойчивости к антибиотикам из-за их неправильного системного применения различные методы местного лечения могут быть эффективными. Цель исследования — сравнить изменения в количестве бактериальной флоры в горле и на поверхности миндалин у пациентов с острым фарингитом после однократного применения местного антибактериального средства в различных формах: таблетки для рассасывания, спрей для горла или раствор для полоскания. Материалы и методы: В данном неинтервенционном наблюдательном исследовании приняли участие 90 взрослых пациентов, которые проходили лечение амбулаторно и страдали от острого фарингита. Пациенты были разделены на три группы: пациенты группы лечения А получали таблетки для рассасывания, содержащие деквалиния хлорид и цинхокаина гидрохлорид; пациенты группы лечения В получали спрей для горла, содержащий растворимый стрептоцид и норсульфазол натрия; пациенты группы лечения С получали порошок Фурасол® 100 мг для полоскания горла, содержащий растворимый фурагин. До и через 20 минут после однократного применения препарата у пациентов брали мазки из зева. Затем проводили микробное исследование полуколичественным методом посева штрихами по квадратам на чашки Петри. Это позволяло оценить количество бактерий до и после применения препарата. Результаты: В ходе исследования в мазках были выявлены четыре патогенных микроорганизма. Наиболее часто встречающимся из них оказался Staphylococcus aureus. Снижение интенсивности роста бактерий после воздействия наблюдалось в 84,6% образцов после лечения C, при этом статистически значимая разница была отмечена как по сравнению с лечением B (57,1%, p < 0,05), так и по сравнению с лечением A (10%, p < 0,05).Также было отмечено значимое различие между группами лечения A и B. Заключение: Результаты исследования показали, что раствор для полоскания горла более эффективно снижает бактериальную нагрузку на слизистую оболочку по сравнению со спреем для горла и таблетками для рассасывания у пациентов с острым фарингитом. Дальнейшие исследования должны быть направлены на изучение эффектов различных лекарственных форм одного и того же антибактериального средства, если таковые имеются.
Ключевые слова: острый фарингит; посев из зева; Streptococcus pyogenes; Staphylococcus aureus; Klebsiella spp.; местное антибактериальное лечение; нитрофурантоин; деквалиний
Вступление
Инфекции верхних дыхательных путей, включая острый фарингит – одна из самых распространённых причин для обращения за медицинской помощью в амбулаторных условиях. Особенно часто такие болезни встречаются у детей до пяти лет [1,2]. Они создают серьёзную нагрузку на систему здравоохранения и приводят к большому количеству пропусков на работе и в школе [3].
Острый фарингит — это воспаление слизистой оболочки глотки [4]. Обычно его вызывают вирусы, такие как риновирус, аденовирус, респираторно-синцитиальный вирус, коронавирус или грипп. Это заболевания, которые проходят самостоятельно и не требуют специального лечения. Однако иногда могут возникнуть осложнения в виде вторичной бактериальной или грибковой инфекции. Реже бактерии могут быть причиной первичного респираторного заболевания. Наиболее распространённой бактерией, вызывающей острый фарингит, является бета-гемолитический стрептококк группы А (Streptococcus pyogenes). Этот микроорганизм обнаруживается у 30% детей и 15% взрослых с болью в горле. Инфекция, вызванная S. pyogenes, должна быть диагностирована и вылечена на ранней стадии. Если её не лечить, она может распространиться из горла и вызвать серьёзные осложнения в других органах, таких как сердце, кровеносные сосуды и почки. Для диагностики бактериального фарингита обычно используется метод посева из зева. Его специфичность составляет 97–100%, а чувствительность — 90–95%. Однако из-за того, что результаты посева приходится ждать долго, в рутинной практике более подходящим может быть экспресс-тест на антиген. Его чувствительность ниже — 70–90% [5], но он позволяет быстрее получить результат. Также могут использоваться другие клинические критерии, например, шкала Centor [6] или шкала McIsaac [7]. Если выявлена бактериальная инфекция, вызванная S. pyogenes, рекомендуется назначить системную антибактериальную терапию [8-11]. Хотя S. pyogenes — наиболее распространённый возбудитель, в инфекциях глотки часто участвуют и другие условно-патогенные бактерии, такие как Staphylococcus aureus и Klebsiella pneumoniae, особенно во вторичных инфекциях после первичного вирусного заболевания.
В условиях растущей устойчивости к противомикробным препаратам, локальная антибактериальная терапия может иметь ряд потенциальных преимуществ. Среди них: высокие и стабильные концентрации препарата непосредственно в очаге инфекции; повышение приверженности лечению; снижение системных побочных эффектов; уменьшение вероятности развития устойчивости к противомикробным препаратам [12]. Такой подход также позволяет минимизировать нецелесообразное использование системных антибактериальных препаратов как у детей, так и у взрослых, что потенциально ограничивает распространение антибиотикорезистентных инфекций [13]. Для борьбы с бактериальными патогенами и предотвращения осложнений, связанных с инфекцией, можно рассмотреть различные альтернативные формы антисептических или антибактериальных препаратов.
Для лечения симптомов бактериальных инфекций горла используются местные средства, такие как спреи, растворы для полоскания и таблетки для рассасывания. Было показано, что полоскание и распыление хлоргексидина предотвращают распространение COVID-19 [14]. Кроме того, таблетки для рассасывания, содержащие как антибактериальные, так и обезболивающие компоненты, могут быть полезны при лечении острого фарингита [15]. В данном исследовании сравниваются три различных метода лечения: таблетки для рассасывания, содержащие деквалиния хлорид, спрей для горла на основе сульфонамида (стрептоцида и норсульфазола натрия) и средство для полоскания на основе нитрофурана (растворимого фурагина). Раствор для полоскания, содержащий растворимый фурагин (действующее вещество), который относится к группе нитрофурановых антибактериальных средств, уже более полувека используется в клинической практике Латвии для лечения боли в горле. Он локализует инфекцию и уменьшает боль в горле, воздействуя на жизнеспособность бактерий, а также обеспечивает патогенетическое лечение острого фарингита [16]. Несмотря на широкое использование местных лекарственных средств, информации о сравнении различных форм препаратов для местного применения при боли в горле недостаточно. Чтобы решить эту проблему, мы провели исследование, в котором сравнили изменения плотности бактериальной обсеменённости горла и слизистой оболочки миндалин у пациентов с острым фарингитом после однократного применения местного антибактериального средства в разных лекарственных формах: таблетки для рассасывания, спрей для горла или раствор для полоскания горла.
Материалы и методы
2.1. Предмет и материалы
В кабинете врача общей практики было проведено неинтервенционное наблюдательное исследование, в котором приняли участие 90 пациентов, посещавших поликлинику. Среди них было 61 женщина и 29 мужчин в возрасте от 19 до 88 лет. Пациентов отбирали по определённым критериям. Главным из них было наличие клинически подтверждённого диагноза острого фарингита, а также назначение одного из трёх методов лечения, которые были предусмотрены протоколом исследования. В исследовании не могли участвовать люди с обострением хронических респираторных заболеваний и/или аллергией в анамнезе, а также те, кто принимал антибиотики в течение последних 24 часов. Перед началом исследования его рассмотрели и одобрили в местном этическом комитете. Все участники дали согласие на использование своих медицинских данных.
В соответствии с протоколом, для лечения острого фарингита предлагались следующие варианты: Декатилен 0,25 мг/0,03 мг, таблетки для рассасывания с действующими веществами деквалиния хлорид, цинхокаина гидрохлорид (производитель «Тева Б.Х.», Хаарлем, Нидерланды), Ингалипт, спрей с действующими веществами стрептоцид растворимый, норсульфазол-натрий (производитель АО «Алтайвитамины», Бийск, Россия) или Фурасол® 100 мг, порошок для приготовления раствора для наружного применения с действующим веществом фурагин растворимый (производитель АО «Олфа», Олайне, Латвия), далее именуемые как Лечение А, В и С соответственно.
2.2. Методы
В рамках исследования были проведены два последовательных микробиологических анализа. Мазок из горла брали до и через 20 минут после однократного приёма назначенного препарата. Этот временной промежуток был выбран как оптимальный, чтобы обеспечить быстрое фармакодинамическое действие всех трёх лекарственных форм, включая время растворения таблетки для рассасывания, и минимизировать нагрузку для пациента. Перед первым забором мазка пациентов просили прополоскать рот. Между забором мазков необходимо было воздержаться от приёма пищи, питья, курения, использования электронных сигарет и жевательной резинки. Клинические образцы высевали на колумбийский кровяной агар («Лиофилхем», Розето дельи Абруцци, Италия) методом штрихового посева на квадрант [17]. Этот полуколичественный экспресс-метод позволяет оценить количество бактерий в образцах и служит основой для дальнейшего анализа [18]. Через 24–48 часов инкубации при температуре 37 °C выросшие колонии (таблица 1) были идентифицированы с помощью анализатора VITEK2 (производитель «биоМерье», Крапонн, Франция). Чтобы сравнить данные in vivo, мы проанализировали, как изменился рост бактерий после воздействия (PGR) (таблица 1). Для этого мы сравнили полуколичественные показатели роста (таблица 1) до и после воздействия для каждого патогена, идентифицированного у пациента. Данные были получены из мазков, взятых до и после воздействия. Все результаты были зафиксированы в стандартных лабораторных рабочих листах и обработаны в соответствии с рутинной лабораторной процедурой.
Таблица 1. Характеристика интенсивности роста бактерий [17].
| Интенсивность роста | Описание |
| (1/2+) скудный рост | 1–5 колоний |
| (1+) небольшой рост | рост только в квадранте 1 * |
| (2+) умеренный рост | рост в квадрантах 1 и 2 * |
| (3+) интенсивный рост | рост в квадрантах 1, 2 и 3 * |
| (4+) очень интенсивный рост | рост во всех 4 квадрантах |
* Не учитывайте несколько колоний в следующем квадранте.
Таблица 2. Сводные данные по снижению роста патогенных видов бактерий после воздействия.
| Лечение A | Лечение B | Лечение C | |||||
| Виды | Парные выборки n | PGR n (%) | Парные выборки n | PGR n (%) | Парные выборки n | PGR n (%) | p < 0,05 |
| S. aureus | 13 | 1 (7,7) | 11 | 5 (45,5) | 14 | 10 (71,4) | A/B, A/C |
| Klebsiella spp. | 4 | 1 (25,0) | 7 | 5 (71,4) | 9 | 9 (100,0) | A/C |
| S. pyogenes | 4 | 0 (0,0) | 3 | 2 (66,7) | 3 | 3 (100,0) | — |
| H. influenzae | 0 | — | 1 | 0 (0,0) | 0 | — | — |
| Всего | 20 | 2 (10) | 21 | 12 (57,1) | 26 | 22 (84,6) | A/B/C |
(PGR) Образцы с замедлением роста после воздействия.
Статистические методы и анализ данных
В ходе исследования не проводился формальный расчёт размера выборки, поскольку оно было направлено на поиск гипотез для будущих исследований. Размер выборки был определён заранее и составлял 30 пациентов в каждой группе. В каждом клиническом образце до воздействия определялось наличие бактерий. После воздействия оценивалось снижение роста патогенных видов бактерий. Данные представлены в таблице 1. Изменения интенсивности роста сравнивались между группами лечения. Все образцы с патогенными бактериями были включены в статистический анализ. Результаты представлены в виде абсолютных и относительных частот. В соответствующих случаях использовался Z-критерий двух пропорций на уровне значимости 5%. Этот критерий использовали специально для сравнения доли образцов, демонстрирующих снижение роста после воздействия (PGR), между тремя группами лечения (A и B, B и C и A и C).
Результаты
Из 90 клинических образцов Staphylococcus aureus был выделен в 38 (42,2%) образцах, Klebsiella spp. – в 20 (22,2%) образцах, Streptococcus pyogenes – в 10 (11,1%) образцах и Haemophilus influenzae – в 1 (1,1%) образце. Из 22 (22,4%) образцов была выделена только нормальная микробиота слизистой оболочки, такая как стрептококки viridans (S. mutans, S. salivarius, S. anginosus, S. mitis, S. sanguinis, S. bovis), Neisseria spp. и Haemophilus parainfluenzae.
В 67 из 90 клинических образцов (74,4%) были обнаружены один из четырёх идентифицированных патогенов. Данные представлены в таблице 2. В 35 из этих 67 образцов (53%) после воздействия наблюдалось снижение роста патогенных микроорганизмов. В остальных 31 образце (47%) интенсивность роста не изменилась. Важно подчеркнуть, что ни в одном из образцов не наблюдалось усиления роста после лечения.
После воздействия (см. таблицу 2) у S. aureus и Klebsiella spp. во всех группах лечения наблюдалось замедление роста, при этом показали значительно отличались между группами лечения B и C и группой лечения A. Для S. pyogenes при лечении B и C также наблюдалось замедление роста, но разница была незначительной. При лечении A такой разницы не было. В одной парной выборке лечение B не показало разницы в отношении H. influenzae.
Индивидуальную интенсивность роста бактерий до и после воздействия для каждого патогенного изолята оценивали с помощью полуколичественного метода штрихового посева на квадрант, описанного в Таблице 1. Плотность бактерий на среде чашки Петри в образцах PGR до воздействия составляла от 4+ до 1+ для S. aureus, от 3+ до 1+ для Klebsiella spp. и от 3+ до 2+ для S. pyogenes. Плотность после воздействия составляла 1+, от 1+ до ½+ и от 2+ до 1+ соответственно (Таблица 3). Количественно в большинстве случаев (72,2%) плотность бактерий снижалась на один квадрант (↓1+); реже (22,2%) — на два квадранта (↓2+); и в одном случае каждый на 0,5 (↓½+) или на три (↓3+) квадранта.
Среднее снижение роста составило около одного квадранта для всех видов лечения, за исключением S.pyogenes при лечении A (без снижения) и S. aureus при лечении B (1,2) и лечении C (1,4) (рисунок 1).
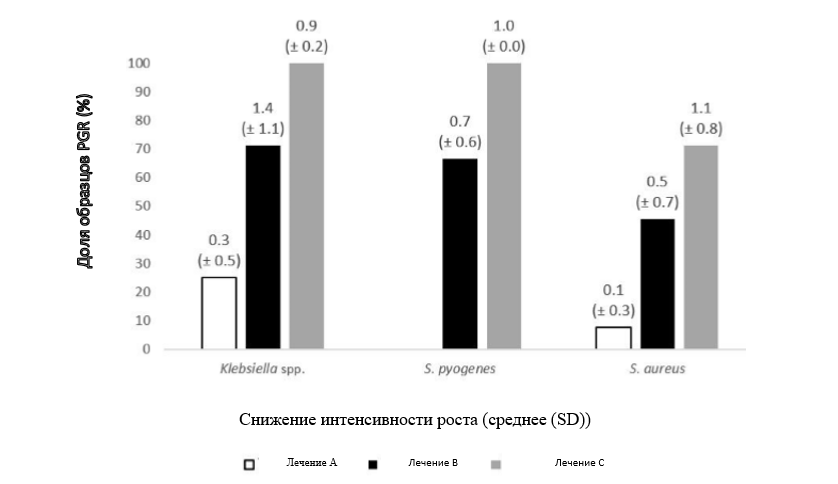
Рисунок 1. Снижение плотности бактерий после воздействия. Среднее снижение роста, измеренное в квадрантах (Q), составило 0,3 (±0,5) после однократного применения лекарственного средства A (таблетки для рассасывания), 1,4 (±1,1) после применения лекарственного средства B (спрей для горла) и 0,9 (±0,2) после применения лекарственного средства C (раствор для полоскания) (виды Klebsiella). Для S. aureus оно составило 0,1 (±0,3), 0,5 (±0,7) и 1,1 (±0,8) соответственно. В случае S. pyogenes пренебрежимо малое снижение роста после воздействия наблюдалось только в группе лечения A (таблетки для рассасывания) и группе лечения C (раствор для полоскания) — 0,3 (±0,5) Q и 0,5 (±0,3) Q соответственно.
Таблица 3. Интенсивность роста патогенных бактерий in vitro в парных клинических образцах.
| Лечение A | Лечение B | Лечение C | ||||||
| Вид | (a) | (b) | Вид | (a) | (b) | Вид | (a) | (b) |
| Klebsiella spp. | 2+ | 2+ | Klebsiella spp. | 4+ | 1+ | Klebsiella spp. | 3+ | 2+ |
| Klebsiella spp. | 2+ | 2+ | Klebsiella spp. | 3+ | 1+ | Klebsiella spp. | 3+ | 2+ |
| Klebsiella spp. | 2+ | 2+ | Klebsiella spp. | 3+ | 1+ | Klebsiella spp. | 3+ | 2+ |
| Klebsiella spp. | 2+ | 1+ | Klebsiella spp. | 1+ | 1+ | Klebsiella spp. | 2+ | 1+ |
| S. pyogenes | 3+ | 3+ | Klebsiella spp. | 2+ | 1+ | Klebsiella spp. | 2+ | 1+ |
| S. pyogenes | 3+ | 3+ | Klebsiella spp. | 2+ | 2+ | Klebsiella spp. | 2+ | 1+ |
| S. pyogenes | 3+ | 3+ | Klebsiella spp. | 3+ | 1+ | Klebsiella spp. | 2+ | 1+ |
| S. pyogenes | 2+ | 2+ | S. pyogenes | 3+ | 2+ | Klebsiella spp. | 2+ | 1+ |
| S. aureus | 3+ | 3+ | S. pyogenes | 2+ | 1+ | Klebsiella spp. | 1+ | 0.5+ |
| S. aureus | 3+ | 3+ | S. pyogenes | 2+ | 2+ | S. pyogenes | 3+ | 2+ |
| S. aureus | 3+ | 3+ | S. aureus | 3+ | 2+ | S. pyogenes | 3+ | 2+ |
| S. aureus | 3+ | 3+ | S. aureus | 3+ | 2+ | S. pyogenes | 2+ | 1+ |
| S. aureus | 3+ | 3+ | S. aureus | 3+ | 2+ | S. aureus | 4+ | 3+ |
| S. aureus | 3+ | 3+ | S. aureus | 3+ | 1+ | S. aureus | 3+ | 2+ |
| S. aureus | 3+ | 3+ | S. aureus | 2+ | 1+ | S. aureus | 3+ | 2+ |
| S. aureus | 2+ | 2+ | S. aureus | 2+ | 2+ | S. aureus | 3+ | 1+ |
| S. aureus | 2+ | 2+ | S. aureus | 2+ | 2+ | S. aureus | 3+ | 1+ |
Таблица 3. Продолжение
| Лечение A | Лечение B | Лечение C | ||||||
| Вид | (a) | (b) | Вид | (a) | (b) | Вид | (a) | (b) |
| S. aureus | 2+ | 2+ | S. aureus | 2+ | 2+ | S. aureus | 3+ | 1+ |
| S. aureus | 2+ | 2+ | S. aureus | 2+ | 2+ | S. aureus | 3+ | 1+ |
| S. aureus | 2+ | 2+ | S. aureus | 2+ | 2+ | S. aureus | 2+ | 2+ |
| S. aureus | 2+ | 1+ | S. aureus | 2+ | 2+ | S. aureus | 2+ | 2+ |
| H. influenzae | 3+ | 3+ | S. aureus | 2+ | 2+ | |||
| (a) — рост до воздействия (b) — рост после воздействия | S. aureus | 2+ | 1+ | |||||
| S. aureus | 2+ | 1+ | ||||||
| S. aureus | 2+ | 1+ | ||||||
| S. aureus | 1+ | 1+ | ||||||
Обсуждение
Патогенные бактерии играют ключевую роль в развитии острого фарингита. Они могут быть как первичной причиной инфекции, так и присоединяться к уже существующему воспалению. S. pyogenes — наиболее распространённый возбудитель бактериального фарингита. Своевременное уничтожение этого микроорганизма помогает снизить заболеваемость и предотвратить возможные осложнения, такие как ревматическая лихорадка и острый гломерулонефрит. Помимо S. pyogenes, существует ряд других бактерий, способных вызывать инфекции верхних дыхательных путей. К ним относятся виды Staphylococcus aureus, Haemophilus influenza, Klebsiella pneumoniae, Proteus, Enterobacter и Citrobacter. Важно отметить, что при вирусном фарингите снижается иммунитет организма, что может привести к развитию вторичных бактериальных осложнений даже при наличии условно-патогенных микроорганизмов [8,19].
В нашем исследовании были выделены следующие виды патогенных микроорганизмов — Staphylococcus aureus, Streptococcus pyogenes, Haemophilus influenza (один изолят вместе с Klebsiella) и Klebsiella spp. (преимущественно Klebsiella pneumoniae).
В целом снижение интенсивности роста бактерий после применения препарата Фурасол® наблюдалось в 84,6% образцов. Была выявлена статистически значимая разница между препаратами Фурасол® и Ингалипт (57,1%, p < 0,05) и препаратом Декатилен (10%, p < 0,05). Также наблюдалась значимая разница между препаратами Декатилен и Ингалипт (p < 0,05). S. aureus — один из главных возбудителей внебольничных и внутрибольничных инфекций, бактериемии и инфекционного эндокардита, а также инфекций кожи, мягких тканей и лёгких [20]. По данным литературы, около 90–100% штаммов S. aureus чувствительны к нитрофуранам [21,22]. В нашем исследовании снижение интенсивности роста бактерий после воздействия наблюдалось в 71,4% клинических образцов в группе препарата Фурасол®, в меньшем количестве образцов в группе препарата Ингалипт (45,5%) и в нескольких образцах в группе препарата Декатилен (7,7%). Хотя сульфаниламиды (действующее вещество препарата Ингалипт) в целом эффективно действуют против стафилококков, их эффективность может быть ниже, чем у препарата Фурасол®. Это может быть связано с различиями в способах применения. Фурасол® в форме раствора для полоскания горла не только обладает антибактериальным действием, но и обеспечивает хороший эффект выполаскивания. В то же время Ингалипт применялся путём распыления, и многие микроорганизмы, особенно находящиеся в биопленках, оставались необработанными.
В общем, стрептококки — это микроорганизмы, которые чувствительны к нитрофуранам. Но научных работ, которые бы изучали чувствительность или устойчивость S. pyogenes, очень мало. Возможно, это связано с тем, что нитрофураны обычно используют для лечения инфекций мочевыводящих путей, где чаще всего встречается S. agalactiae. В нашем исследовании мы обнаружили, что содержание S. pyogenes снизилось во всех образцах в группе, где применяли Фурасол®, (100%). В группе, где использовали Ингалипт, содержание S. pyogenes снизилось в 66,7% образцах. А вот Декатилен не оказал никакого эффекта.
В последнее время вызывает тревогу увеличение количества случаев заражения инфекциями, вызванными K. pneumoniae, а также повышение уровня устойчивости к ним. Устойчивость к нитрофурантоину среди штаммов K. pneumoniae, выделенных из различных биологических материалов (кровь, моча, мокрота и шейка матки), варьируется от 13 до 33% [23,24]. Во всём мире наблюдается стабильная устойчивость к сульфаниламидам [25]. Устойчивость штаммов K. pneumoniae, обнаруженных в горле, невысока. В нашем исследовании было установлено, что Фурасол® эффективен в отношении всех изолятов (100%), в то время как Ингалипт показал результат в 71,4% случаев, а Декатилен — только в 25%. Важно отметить, что способ применения препарата может влиять на его эффективность – смывание «поверхностного патогена» вместо воздействия на бактерии, поразившие внутренние ткани и органы.
Значительные различия в эффективности можно объяснить особенностями фармакодинамики трёх лекарственных форм. Препарат С, который представляет собой раствор для полоскания, демонстрирует высокую эффективность благодаря своему двойному действию. Он не только уничтожает бактерии с помощью действующего вещества фурагин растворимый, но и механически очищает слизистую оболочку при полоскании. Этот механический эффект, вероятно, позволяет удалить большое количество неприкрепившихся бактерий, слизи и других загрязнений с поверхности слизистой оболочки, что не характерно для других форм препаратов. В отличие от этого, лечение А, основанное на применении таблеток для рассасывания, предполагает длительный контакт с поверхностью, так как таблетки растворяются, позволяя антисептику (деквалинию) проявить своё действие. Результаты нашего исследования показали, что эффективность лечения А очень низкая (снижение 10%), что может свидетельствовать о том, что этот механизм менее эффективен в условиях in vivo, возможно, из-за ограниченной способности средства проникать через биоплёнки в глотке. Это является известным ограничением эффективности действия деквалиния. Лечение В, представленное спреем для горла, занимает промежуточное положение между двумя другими методами. Препарат применяется местно, но не обеспечивает ни полного механического промывания горла, ни длительного контакта, как таблетки для рассасывания.
Бактерия H. influenza была обнаружена только в одном образце в группе, получавшей Ингалипт, и не показала признаков снижения роста после применения спрея для горла.
В составе таблеток для рассасывания содержится вещество под названием деквалиний. Оно способно связываться с поверхностью бактериальной клетки и проникать сквозь её оболочку, нарушая её целостность. Попадая внутрь микроорганизма, деквалиний денатурирует белки, которые участвуют в процессах дыхания и гликолиза. Это приводит к нарушению обмена веществ и синтеза белка в микроорганизме. Кроме того, деквалиний препятствует образованию АТФ в митохондриях и блокирует метаболизм глюкозы [26]. Благодаря этим механизмам действия, развитие устойчивости к антимикробным препаратам становится маловероятным [27]. Таким образом, местное использование препарата при лечении фарингита должно было показать хороший антибактериальный эффект против бактерий, которые были выделены в ходе нашего исследования. Но эффект оказался довольно слабым. Вероятно, это связано с тем, что микроорганизмы, образующие биоплёнки, играют важную роль в развитии бактериальных инфекций полости рта и глотки. Однако деквалиний может быть недостаточно эффективен или совсем неэффективен против зрелых биоплёнок [28].
Все три препарата, которые мы использовали в нашем исследовании, показали антибактериальную активность. Однако более высокая эффективность препарата Фурасол® может быть связана с его способом применения. Этот препарат не только оказывает антибактериальное действие, но и обладает «промывающим» эффектом, что делает его более эффективным, чем спрей для горла и таблетки для рассасывания. В литературе мы нашли только одну статью, в которой сравниваются различные лекарственные формы, используемые для лечения бактериального фарингита. В этой статье не было обнаружено различий между препаратами [29]. Однако есть данные, которые подтверждают, что полоскание горла помогает ограничить инфекции верхних дыхательных путей, сократить продолжительность заболевания, уменьшить потребность в системном применении лекарств и снизить вероятность передачи инфекции от человека к человеку [30, 31].
При анализе клинической значимости полученных результатов важно принимать во внимание и другие аспекты. Например, следует учитывать, сколько времени потребуется для снижения концентрации бактерий, как это повлияет на восстановление слизистой оболочки, какой эффект оказывают препараты на её увлажнение и смягчение. Также важно учитывать, как часто нужно применять лекарство, и предпочтения пациентов. Однако при оценке результатов исследования нужно учитывать и его ограничения. Поскольку в ходе исследования не применялся метод «слепого» контроля, существует риск систематической ошибки на этапе микробиологической оценки, особенно при полуколичественном определении интенсивности роста. Кроме того, поскольку это было наблюдательное исследование, точный объём и продолжительность полоскания горла в группе лечения C не были строго стандартизированы или зафиксированы, что также является ограничением.
Заключение
В ходе выполненного нами исследования было установлено, что раствор для полоскания горла демонстрирует более значительное уменьшение количества бактерий на поверхности слизистой оболочки глотки и миндалин у людей с острым фарингитом по сравнению с использованием спрея для горла или таблеток для рассасывания. Дальнейшие исследования должны быть сосредоточены на изучении различных лекарственных форм одного и того же антибактериального препарата, если таковые существуют.
Вклад авторов: разработка концепции (А.Р.); методология (А.Р.); формальный анализ (Г.Д.); исследование (А.Р., С.Г., А.Т., К.В., О.З. и Т.С.); ресурсы (С.Г.); контроль данных (А.Р. и С.Г.); написание — подготовка первоначального черновика (Г.Д. и Л.Б.); написание — рецензирование и редактирование (А.Р.); визуализация (Г.Д.); контроль (А.Р. и С.Г.); администрирование проекта (А.Р. и С.Г.). Все авторы ознакомились с опубликованной версией рукописи и согласились с ней.
Финансирование: Проект выполнен при поддержке компании АО «Олфа».
Заявление Институционального наблюдательного совета: Исследование проведено в соответствии с принципами Хельсинкской декларации и одобрено Комитетом по этике Рижского университета имени Страдыня (Решение № 2-PEK-4/492/2023 от 25 июля 2023 г.).
Заявление об информированном согласии: Информированное согласие получено от всех участников исследования.
Заявление о доступности данных: Данные содержатся в статье.
Конфликт интересов: Гуна Дансоне и Лига Балоде являются сотрудниками АО «Олфа», производящего раствор для наружного применения Фурасол®. Все остальные авторы заявляют об отсутствии конфликта интересов в отношении публикации данной статьи.
Отказ от ответственности/Примечание издателя: заявления, мнения и данные, содержащиеся во всех публикациях, принадлежат исключительно отдельным авторам и соавторам, а не MDPI и/или редакторам. MDPI и/или редакторы не несут ответственности за любой ущерб, причиненный людям или имуществу в результате использования любых идей, методов, инструкций или продуктов, указанных в материалах.
Источники:
- Finley, C.R.; Chan, D.S.; Garrison, S.; Korownyk, C.; Kolber, M.R.; Campbell, S.; Eurich, D.T.; Lindblad, A.J.; Vandermeer, B.; Allan, G.M. What are the most common conditions in primary care? Can. Fam. Physician 2018, 64, 832–840.
- Jin, X.; Ren, J.; Li, R.; Gao, Y.; Zhang, H.; Li, J.; Zhang, J.; Wang, X.; Wang, G. Global burden of upper respiratory infections in 204 countries and territories, from 1990 to 2019. E Clin. Med. 2021, 37, 100986.
- Pfoh, E.; Wessels, M.R.; Goldmann, D.; Lee, G.M. Burden and economic cost of group A streptococcal pharyngitis. Pediatrics 2008, 121, 229–234.
- Calderaro, A.; Buttrini, M.; Farina, B.; Montecchini, S.; De Conto, F.; Chezzi, C. Respiratory tract infections and laboratory diagnostic methods: A review with a focus on syndromic panel-based assays. Microorganisms 2022, 10, 1856.
- Shulman, S.T.; Bisno, A.L.; Clegg, H.W.; Gerber, M.A.; Kaplan, E.L.; Lee, G.; Martin, J.M.; Van Beneden, C. Clinical practice guideline for the diagnosis and management of group A streptococcal pharyngitis: 2012 update by the Infectious diseases society of America. Clin. Infect. Diseases 2012, 55, e86–e102.
- NICE Guidance. Rapid Tests for Group a Streptococcal Infections in People with a Sore Throat; NICE: Hoboken, NJ, USA, 2019.
- Reinholdt, K.B.; Rusan, M.; Hansen, P.R.; Klug, T.E. Management of sore throat in Danish general practices. BMC Fam. Pract. 2019, 20, 75.
- Hendaus, M.A.; Jomha, F.A.; Alhammadi, A.H. Virus-induced secondary bacterial infection: A concise review. Ther. Clin. Risk Manag. 2015, 11, 1265–1271.
- Alcaide, M.L.; Bisko, A.L. Pharyngitis and epiglottitis. Infect. Dis. Clin. N. Am. 2007, 21, 449–469.
- Sykes, E.A.; Wu, V.; Beyea, M.M.; Simpson, M.T.W.; Beyea, J.A. Pharyngitis: Approach to diagnosis and treatment. Can. Fam. Physician 2020, 66, 251–257.
- Pichichero, M.E. Treatment and Prevention of Streptococcal Pharyngitis in Adults and Children; UpToDate: Waltham, MA, USA, 2025.
- Ray, P.; Singh, S.; Gupta, S. Topical antimicrobial therapy: Current status and challenges. Indian J. Med. Microbiol. 2019, 37, 299–308.
- Fleming-Dutra, K.E.; Hersh, A.L.; Shapiro, D.J.; Bartoces, M.; Enns, E.A.; File, T.M.; Finkelstein, J.A.; Gerber, J.S.; Hyun, D.Y.; Linder, J.A.; et al. Prevalence of inappropriate antibiotic prescriptions among US ambulatory care visits, 2010–2011. JAMA 2016, 315, 1864–1873.
- Huang, Y.H.; Huang, J.T. Use of chlorhexidine to eradicate oropharyngeal SARS-CoV-2 in COVID-19 patients. J. Med. Virol. 2021, 93, 4370–4373.
- Palm, J.; Fuchs, K.; Stammer, H.; Schumacher-Stimpfl, A.; Milde, J.; DoriPha Investigators. Efficacy and safety of a triple active sore throat lozenge in the treatment of patients with acute pharyngitis: Results of a multi-centre, randomized, placebo-controlled, double-blind, parallel-group trial (DoriPha). Int. J. Clin. Pract. 2018, 72, e13272.
- Wolford, R.W.; Goyal, A.; Belgam Syed, S.Y.; Schaefer, T.J. Pharyngitis. [Updated 2023 May 1]. In StatPearls [Internet]; StatPearls Publishing: Treasure Island, FL, USA, 2025. Available online: https://www.ncbi.nlm.nih.gov/books/NBK519550/ (accessed on 10 September 2025).
- Leber, A.L. Clinical Microbiology Procedures Handbook, 4th ed.; ASM Press: Washington, DC, USA, 2016.
- Cox, N.A.; Richardson, L.J.; Cosby, D.E.; Berrang, M.E.; Wilson, J.L.; Harrison, M.A. A four-quadrant sequential streak technique to evaluate Campylobacter selective broths for suppressing background flora in broiler carcass rinses. J. Food Saf. 2017, 37, e12311.
- Manohar, P.; Loh, B.; Athira, S.; Nachimuthu, R.; Hua, X.; Welburn, S.C.; Leptihn, S. Secondary bacterial infections during pulmonary viral disease: Phage therapeutics as alternatives to antibiotics? Front. Microbiol. 2020, 11, 1434.
- González-García, S.; Hamdan-Partida, A.; Bustos-Hamdan, A.; Bustos-Martínez, J. Factors of nasopharynx that favor the colonization and persistence of Staphyloccocus aureus. In Pharynx—Diagnosis and Treatment; IntechOpen: London, UK, 2021.
- An, N.; Hai, L.H.L.; Luong, V.H.; Vinh, N.T.H.; Hoa, P.Q.; Hung, L.; Son, N.T.; Hong, L.T.; Hung, D.V.; Kien, H.T.; et al. Antimicrobial resistance patterns of Staphylococcus aureus isolated at a General Hospital in Vietnam between 2014 and 2021. Infect. Drug Resist. 2024, 17, 259–273.
- Gitau, W.; Masika, M.; Musyoki, M.; Museve, B.; Mutwiri, T. Antimicrobial susceptibility pattern of Staphyloccocus aureus isolates from clinical specimens at Kenyatta National Hospital. BMC Res. Notes 2018, 11, 226.
- Li, G.; Zhao, S.; Wang, S.; Sun, Y.; Zhou, Y.; Pan, X. A 7-year surveillance of the drug resistance in Klebsiella pneumoniae from primary health care center. Ann. Clin. Microbiol. Antimicrob. 2019, 18, 34.
- Park, K.-S.; Kim, D.R.; Baek, J.Y.; Shin, A.; Kim, K.-R.; Park, H.; Son, S.; Cho, H.; Kim, Y.-J. Susceptibility to fosfomycin and nitrofurantoin of ESBL-positive Escherichia coli and Klebsiella pneumoniae isolated from urine of pediatric patients. J. Korean Med. Sci. 2023, 48, e361.
- Asri, N.A.M.; Ahmad, S.; Mohamud, R.; Hanafi, N.M.; Zaidi, N.F.M.; Irekeola, A.A.; Shueb, R.H.; Yee, L.C.; Noor, N.M.; Mustafa, F.H.; et al. Global prevalence of nosocomial multidrug-resistant Klebsiella pneumoniae: A systematic review and meta-analysis. Antibiotics 2021, 10, 1508.
- Dequalinium. Available online: https://go.drugbank.com/drugs/DB04209 (accessed on 25 September 2024).
- Raba, G.; Ďurkech, A.; Malík, T.; Bassfeld, D.; Grob, P.; Hurtado-Chong, A.; Botta, S.; Sach, A.; Golańska-Wróblewska, M.; Paškala, M.; et al. Efficacy of dequalinium chloride vs. metronidazole for the treatment of bacterial vaginosis: A randomized clinical trial. JAMA Netw. Open 2024, 7, e248661.
- Schwarz, S.R.; Hirsch, S.; Hiergeist, A.; Kirschneck, C.; Muehler, D.; Hiller, K.-A.; Maisch, T.; Al-Ahmad, A.; Gessner, A.; Buchalla, W.; et al. Limited antimicrobial efficacy of oral care antiseptics in microcosm biofilms and phenotypic adaptation of bacteria upon repeated exposure. Clin. Oral. Investig. 2021, 25, 2939–2950.
- Radkova, E.; Burova, N.; Bychkova, V.; DeVito, R. Efficacy of flurbiprofen 8.75 mg delivered as a spray or lozenge in patients with sore throat due to upper respiratory tract infection: A randomized, non-inferiority trial in the Russian Federation. J. Pain. Res. 2017, 10, 1591–1600.
- Satomura, K.; Kitamura, T.; Kawamura, T.; Shimbo, T.; Watanabe, M.; Kamei, M.; Takano, Y.; Tamakoshi, A. Prevention of upper respiratory tract infections by gargling: A randomized trial. Am. J. Prev. Med. 2005, 29, 302–307.
- Ramalingam, S.; Graham, C.; Dove, J.; Morrice, L.; Sheikh, A. A pilot, open labelled, randomized controlled trial of hypertonic saline nasal irrigation and gargling for the common cold. Sci. Rep. 2019, 9, 1015.
Источник статьи: Рейнис, А.; Дансоне, Г.; Балоде, Л.; Гинтере, С.; Толстикс, А.; Вербовенко, К.; Зашибаевс, О.; Сафина, Т. Влияние различных местных антибактериальных препаратов на плотность бактерий на слизистой оболочке глотки и миндалин у пациентов с острым фарингитом. Medicina 2025, 61, 2100. https://doi.org/10.3390/medicina61122100
Цель исследования — сравнить изменения в количестве бактериальной флоры в горле и на поверхности миндалин у пациентов с острым фарингитом после однократного применения местного антибактериального средства в различных формах.
Этот контент предназначен только для зарегистрированных пользователей. Пожалуйста, войдите или зарегистрируйтесь.
