Инсульт — вторая по частоте причина смертности в мире1
За последние 30 лет возросли1:


Когда холин перестает быть полезным: обратная сторона «добавок для мозга»
Экзогенный холин назначается в виде добавок, например, L-альфа-глицерилфосфорилхолина, для профилактики деменции и дисфункции холинергической системы.
Попадая в организм, холин при участии кишечной микрофлоры синтезируется в триметиламиноксид (ТМАО).
В чем же опасность метаболита ТМАО2?
- Усиливает образование пенистых клеток и рост атеросклеротических бляшек.
- Является одной из причин эндотелиальной дисфункции — воспаления эндотелия.
- Повышает агрегацию тромбоцитов и риск ишемического инсульта.
L-альфа-глицерилфосфорилхолин (холина альфосцерат): что говорит наука о приеме экзогенного холина3
Результаты 10-летнего когортного исследования с участием более 12 млн. человек показали3:
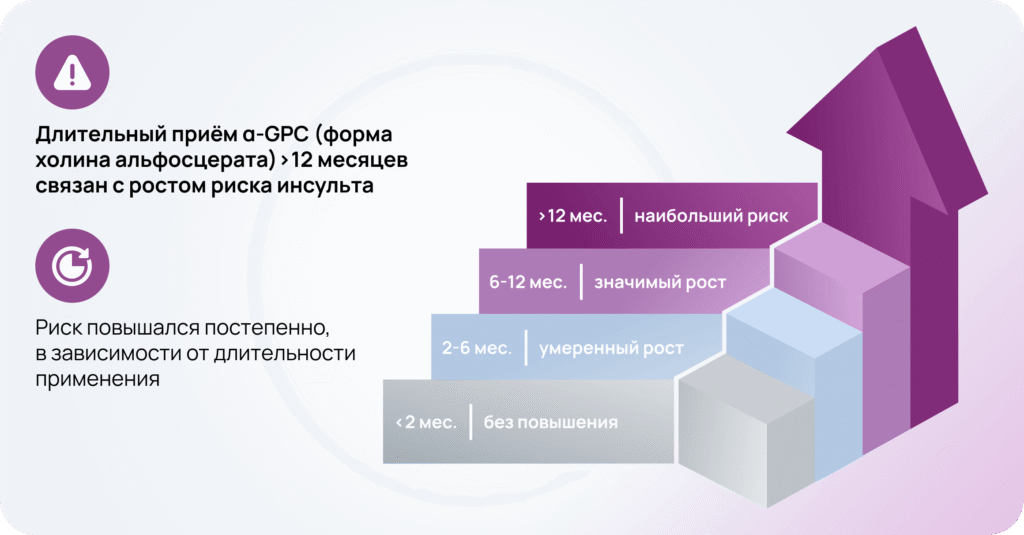

Назначение донаторов холина пациентам с сосудистым риском требует индивидуального подхода с учётом метаболических особенностей и состава кишечной микробиоты; неконтролируемое использование БАДов и препаратов с высокими дозами холина следует избегать.
Какую безопасную поддержку холинергической регуляции подобрать для пациентов, перенесших инсульт?
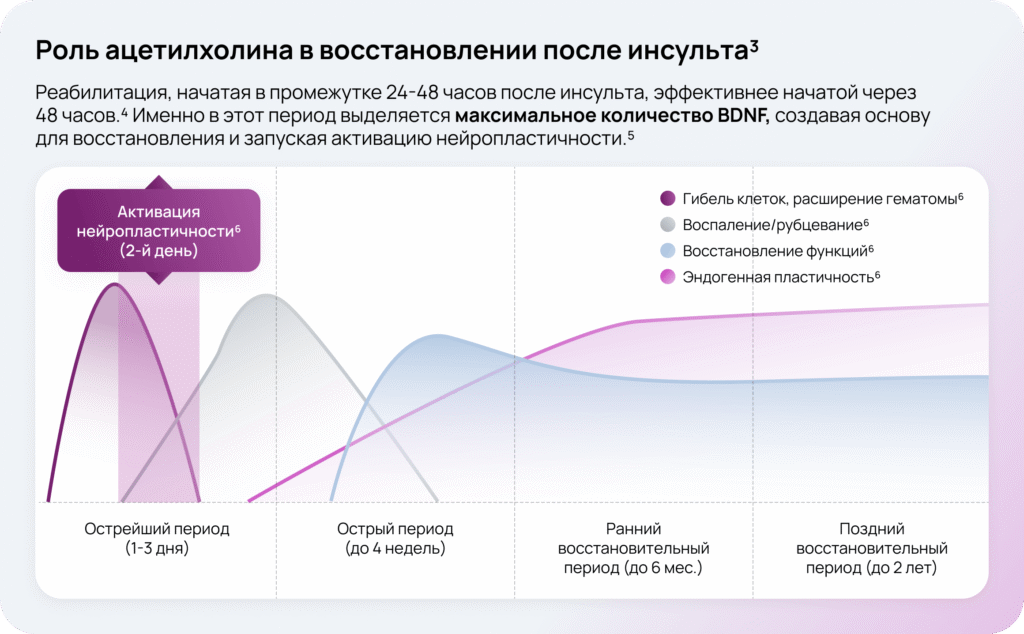
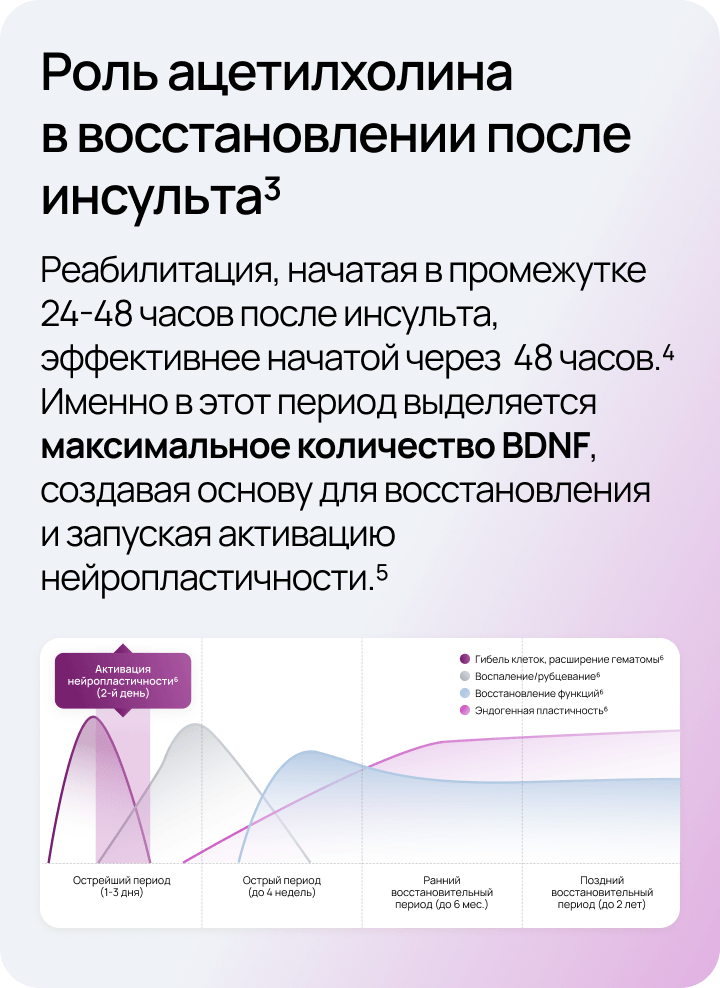
Ацетилхолин через мускариновые и никотиновые рецепторы, особенно α7-nAChR, активирует внутриклеточные сигнальные каскады, которые запускают транскрипцию гена BDNF5.
Нейромидин® (ипидакрин), обратимый ингибитор ацетилхолинэстеразы, повышает концентрацию эндогенного ацетилхолина в синапсах, блокируя его распад 11.
Актуальная стратегия восстановления функций после инсульта


В рандомизированном исследовании, включавшем пациентов с ишемическим инсультом каротидного бассейна, добавление Нейромидин® к стандартной терапии способствовало более выраженному восстановлению неврологических функций по сравнению с контрольной группой. Препарат хорошо переносился, побочных эффектов не зафиксировано9.
Общая оценка эффективности лечения
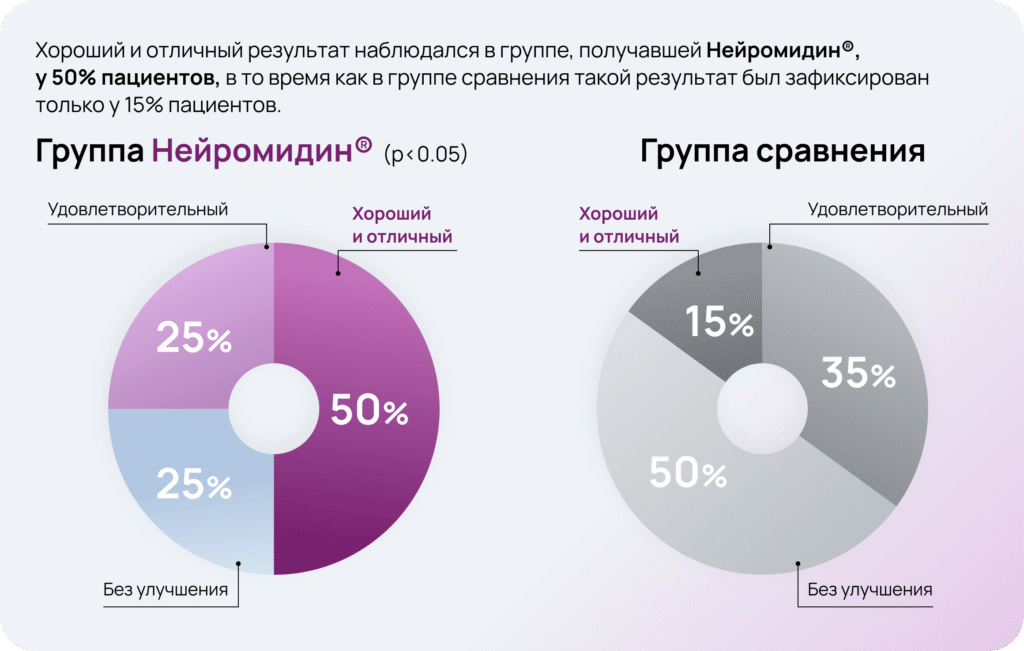
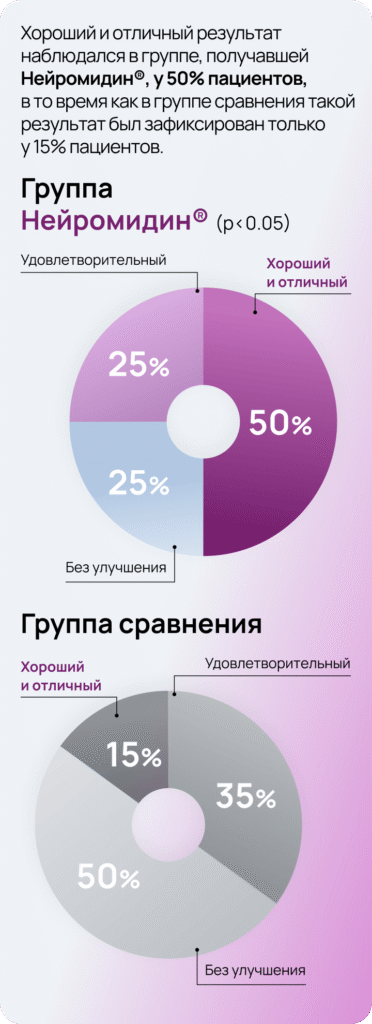
При лечении препаратом Нейромидин® отмечалось постепенное уменьшение выраженности неврологической симптоматики, и к 80-м суткам после инсульта неврологический статус по СШИ улучшился в среднем на 22%. Тяжесть инсульта стала соответствовать лёгкой степени.
При оценке динамики пациентов, получавших только базисную терапию, статистически значимых различий между исходным уровнем и спустя 80 дней после начала терапии не выявлено.
Схема назначения препарата Нейромидин® в остром периоде инсульта10,11
- В течение 14 дней: в/м раствор 15 мг/мл по 1 мл 2 раза в сутки.
- Затем продолжают терапию, перейдя на таблетированную форму: 40 мг в сутки (по 1 таблетке 2 раза в сутки) в течение 45–90 дней.
В острый период инсульта Нейромидин® включают в базовую терапию только после стабилизации состояния пациента.
ТМАО — триметиламиноксид, ТМА — триметиламин, α-GPC — L-альфа-глицерилфосфорилхолин, БАД — биологически активная добавка, BDNF (brain-derived neurotrophic factor) — белок мозгового нейротрофического фактора, ЦНС — центральная нервная система, ПНС — периферическая нервная система, СШИ — скандинавская шкала инсульта.
- GBD 2019 Stroke Collaborators. «Global, regional, and national burden of stroke and its risk factors, 1990–2019: a systematic analysis for the Global Burden of Disease Study 2019.» Lancet Neurol., vol. 20, 2021, pp. 795–820. Published Online September 3, 2021. doi: 10.1016/S1474-4422(21)00252-0.
- Zhu Y. et al. Gut microbiota in atherosclerosis: focus on trimethylamine N-oxide. APMIS, 2020; 128(5):353-366. DOI: 10.1111/apm.13038 JAMA Netw Open Published Online: November 24, 2021;4;(11):e2136008. doi:10.1001/jamanetworkopen.2021.36008.
- Lee G, Choi S, Chang J, Choi D, Son JS, Kim K, Kim SM, Jeong S, Park SM. Association of L-α Glycerylphosphorylcholine With Subsequent Stroke Risk After 10 Years. JAMA Netw Open. 2021 Nov 1;4(11):e2136008. doi: 10.1001/jamanetworkopen.2021.36008. PMID: 34817582; PMCID: PMC8613599.
- Otokita S. et al. Impact of rehabilitation start time on functional outcomes after stroke. Journal of Rehabilitation Medicine. 2021; 53(1): jrm00145. doi: 10.2340/16501977-2775
- Liu Yi et al. Early Rehabilitation after Acute Stroke: The Golden Recovery Period. Acta Neurologica Taiwanica, 2022.
- Адаптировано по материалам: Bernhardt J., Hayward K.S., Kwakkel G. et al. Agreed definitions and a shared vision for new standards in stroke recovery research: The Stroke Recovery and Rehabilitation Roundtable Taskforce. International Journal of Stroke. 2017; 12(5): 444–450. doi: 10.1177/1747493017711816
- Fernandes C.C. et al. Postsynaptic action of brain-derived neurotrophic factor attenuates alpha7 nicotinic acetylcholine receptor-mediated responses in hippocampal interneurons. Journal of Neuroscience. 2008; 28(21):5611–8. doi: 10.1523/JNEUROSCI.5378-07.2008 PMID: 18495895; PMCID: PMC6670615.
- Bathina S., Undurti N.D. Brain-derived neurotrophic factor and its clinical implications. Archives of Medical Science. 2015; 11(6):1164–78. doi: 10.5114/aoms.2015.56342
- Maximova M.Yu. et al. Neyromidin in ischemic stroke. Journal of Neurology and Psychiatry. 2013; 3.
- Дамулин И. В. с соавт. Нейромидин® в клинической практике. 2-е изд., перераб. и доп. — М.: ООО «Медицинское информационное агентство», 2016. — 60 стр. ISBN 978-5-8948-1942-6.
- Инструкция по медицинскому применению лекарственного средства Нейромидин®.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Сигнал покоя: ацетилхолин в действии
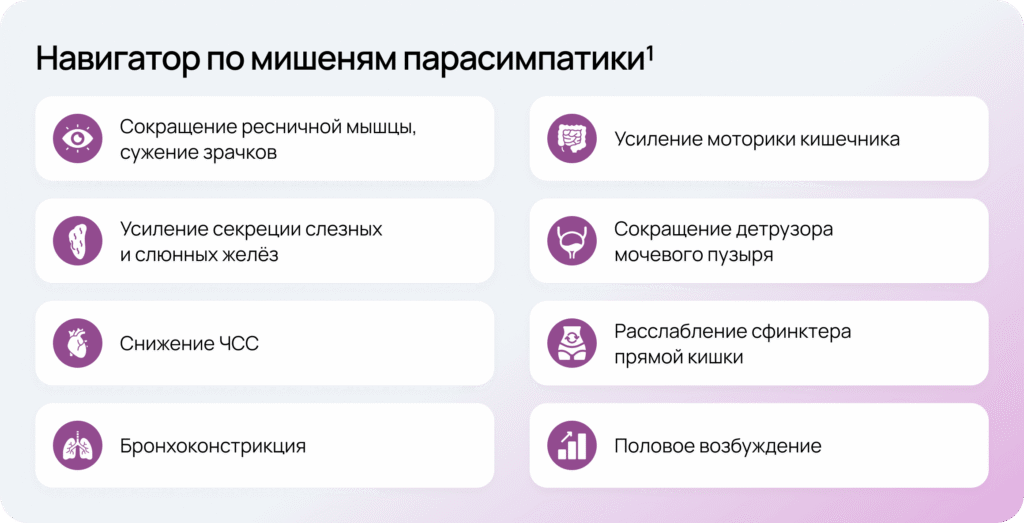
Ацетилхолин — основной нейротрансмиттер парасимпатической системы. Сигнал проходит через никотиновые рецепторы ганглиев, а затем через мускариновые рецепторы периферических органов, регулируя выраженность автономных функций1.
При ослаблении холинергической передачи формируется спектр проявлений дизавтономии — прежде всего ортостатические жалобы, желудочно-кишечные симптомы, урологические нарушения, а также проблемы секреции, нередко сочетающиеся с нарушениями зрачковых реакций и терморегуляции.

Свежий взгляд на диагностику нарушений2: COMPASS-31
Уникальным компонентом скрининга нарушений является Composite Autonomic Symptom Score — 31 (COMPASS-31)3, он помогает эффективно оценить наличие и локализацию нарушения в работе систем органов, а последующее целенаправленное обследование уточняет дисфункцию и ее степень.


Практическое применение: оптимизируем подход к диагностике
- COMPASS-31 — удобный инструмент оценки вегетативных симптомов, позволяющий определить степень тяжести дизавтономии и локализацию
- Опросник оптимизирует клинический поиск и динамическую оценку состояния пациентов с вегетативной недостаточностью
Ацетилхолин: активатор холинергического пути
Ацетилхолин участвует в передаче импульса в нервной системе, а также играет ключевую роль в регуляции работы систем органов4. Даже незначительные нарушения его уровня могут способствовать развитию хронических патологических процессов4.
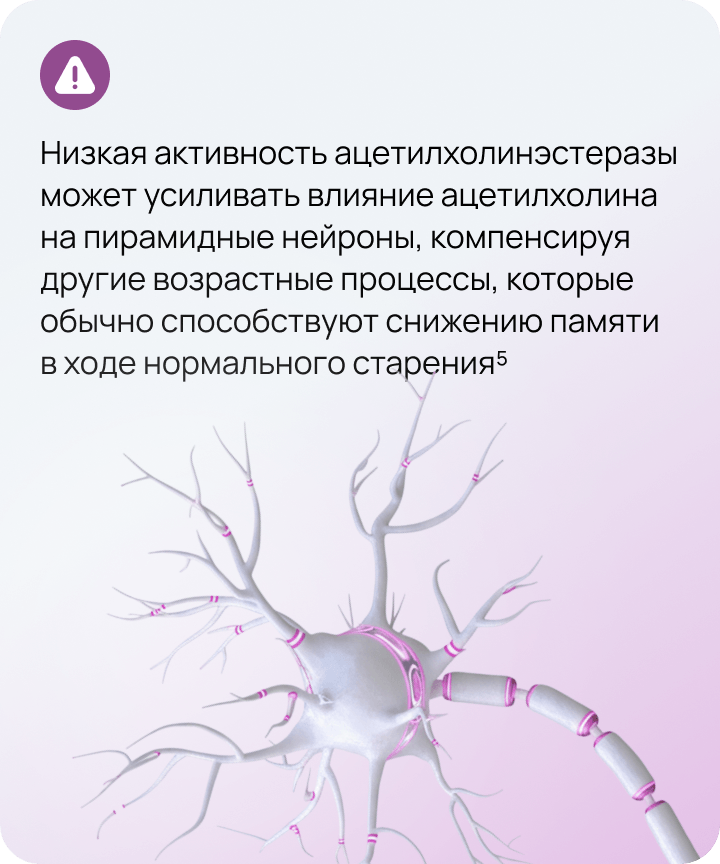
Низкий уровень холинэстеразы один из признаков суперэйджеров5
Суперэйджеры — люди старше 80 лет, чьи когнитивные способности на среднестатистическом уровне людей среднего возраста.

Нейромидин® (ипидакрин)
Обратимый ингибитор ацетилхолинэстеразы, усиливает холинергеческую передачу4,8 в парасимпатической системе.
Увеличение концентрации ключевого нейротрансмиттера ацетилхолина обеспечивает:
- Восстановление когнитивного резерва6
- Восстановление нервно-мышечной передачи
- Регенерацию поврежденных нервных волокон7,8


COMPASS-31 — Composite Autonomic Symptom Score — 31, комплексная шкала оценки симптомов 6 автономных доменов; ЦНС — центральная нервная система; ПНС — периферическая нервная система, ЧСС — частота сердечных сокращений.
- LeBouef T, Yaker Z, Whited L. Physiology, Autonomic Nervous System. [Updated 2023 May 1]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK538516/
- Sánchez-Manso JC, Gujarathi R, Varacallo MA. Autonomic Dysfunction. [Updated 2023 Aug 4]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK430888/
- Sletten, D. M., Suarez, G. A., & Low, P. A. (2012b). COMPASS 31: A Refined and Abbreviated Composite Autonomic Symptom Score. Mayo Clinic Proceedings, 87(12), 1196–1201. Accessed: https://www.hattrevaluationtools.eu/compass-31/
- Mohan, V., Kaushik, D., & Arora, K. (2023). Role of Acetylcholine in Chronic Diseases. IntechOpen. doi: 10.5772/intechopen.110663
- Janeczek M, Gefen T, Samimi M, Kim G, Weintraub S, Bigio E, Rogalski E, Mesulam MM, Geula C. Variations in Acetylcholinesterase Activity within Human Cortical Pyramidal Neurons Across Age and Cognitive Trajectories. Cereb Cortex. 2018 Apr 1;28(4):1329-1337. doi: 10.1093/cercor/bhx047. PMID: 28334147; PMCID: PMC6059146.
- Дамулин И.В. с соавт. Нейромидин в клинической практике. 2-с изд., перераб. и доп. — М.: ООО «Медицинское информационное агентство». 2016. – 60 с. ISDB 978-5-8948-1942-6.
- Живолупов C.А., Самарцев И.Н. Центральные механизмы терапевтической эффективности нейромидина в лечении травматических поражений периферической нервной системы. Журнал неврологии и психиатрии им. С.С. Корсакова. 2010; 110(3): 25–30.
- Самарцев И.Н., Живолупов С.А., Воробьева М.Н., Паршин М.С., Нажмудинов Р.З. Оптимизация дифференциальной диагностики и терапии вертеброгенной шейной радикулопатии (исследование ШЕРПА). Журнал неврологии и психиатрии им. С.С. Корсакова. 2020; 120(9):37-46.
- Инструкция по медицинскому применению лекарственного средства Нейромидин®, таблетки 20 г.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Сон — зеркало когнитивного здоровья
Часто мы рассматриваем нарушения сна у пациентов с когнитивными расстройствами как параллельно текущие коморбидные состояния.
Однако исследования показывают: специфические нарушения сна могут являться ранними предикторами тяжёлых нейродегенеративных заболеваний, таких как болезнь Альцгеймера или Паркинсона, возникая за 10–15 лет до первых специфических клинических признаков1.


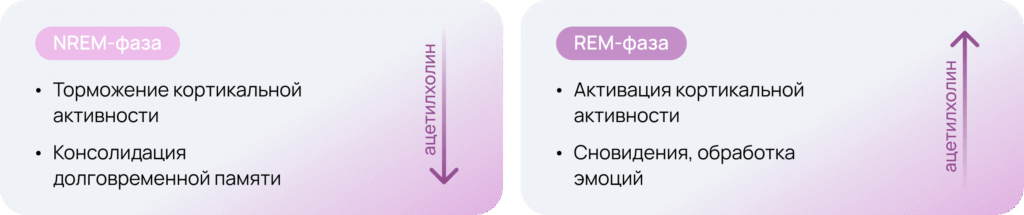
Холинергическая система как переключатель между NREM и REM
Холинергическая активность достигает максимума во время фазы быстрого сна (REM) — в отличие от медленного сна (NREM) и бодрствования — когда активность других нейромедиаторных систем существенно снижена3.
Холинергические нейроны базальных отделов переднего мозга проецируются в неокортекс, вызывая активацию коры, характерную для REM-фазы4.

Расстройство поведения в быстрой фазе сна
Одним из ранних признаков нейродегенерации считается расстройство поведения в фазе быстрого сна (RBD). Исследования показывают, что это состояние нередко предшествует развитию болезни Паркинсона и других заболеваний, связанных с накоплением α-синуклеина5.
У ~50% пациентов с идиопатическим RBD расстройством развивается паркинсонический синдром в течение 10 лет, а у 81–90% —нейродегенеративное заболевание5.


Для подтверждённого диагноза RBD должны быть выполнены все критерии6
- Повторяющиеся эпизоды вокализаций во сне и/или сложных движений.
- Эти эпизоды зафиксированы с помощью полисомнографии как происходящие во время REM-фазы сна.
- Полисомнография демонстрирует REM-сон без атонии, то есть отсутствие нормального мышечного расслабления во время фазы быстрого сна.
- Полисомнография демонстрирует REM-сон без атонии, то есть отсутствие нормального мышечного расслабления во время фазы быстрого сна.
Регуляция холинергии для защиты когнитивного резерва
Обратимые ингибиторы ацетилхолинстеразы входят в актуальные мировые рекомендации по коррекции RBD7.
Они оказывают благоприятное влияние на стимуляцию холинергических нейронов, что, соответственно, влияет на продолжительноть REM-фазы и когнитивные функции в целом.
Препаратом, стимулирующим выброс ацетилхолина, является Нейромидин® (ипидакрин), он положительно влияет на улучшение когнитивных функций, восстанавливая и защищая нейроны от повреждения, вызванного нейровоспалением и нейродегенерацией8.
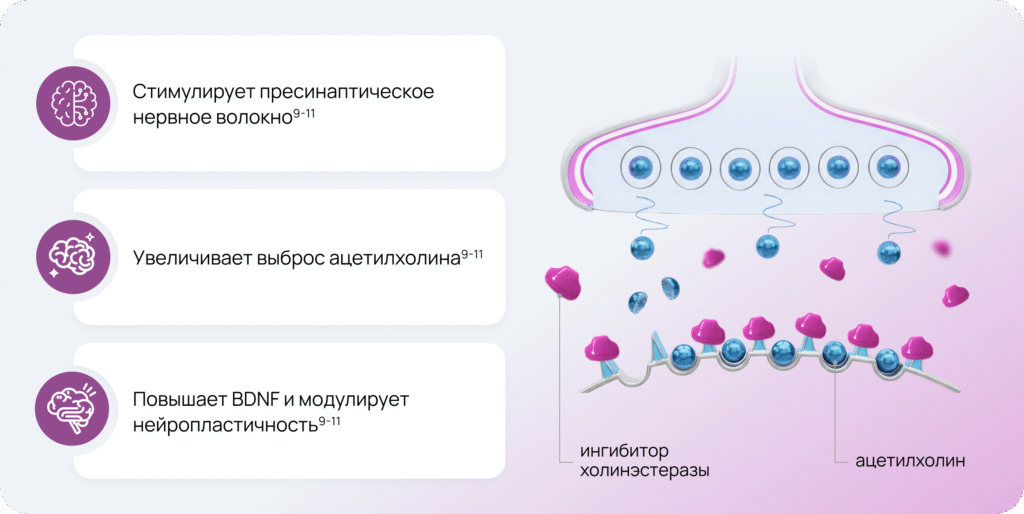

Причины выбрать Нейромидин® при нарушении памяти


NREM — Non-rapid eye movement, фаза медленного сна; REM — Rapid eye movement, фаза быстрого сна; BDNF — Brain-derived neurotrophic factor, нейтротропный фактор мозга; RBD — REM sleep behavior disorder, расстройства поведения в фазе быстрого сна.
- Mander BA, Winer JR, Jagust WJ, Walker MP. Sleep: A Novel Mechanistic Pathway, Biomarker, and Treatment Target in the Pathology of Alzheimer’s Disease? Trends Neurosci. 2016 Aug;39(8):552–566. doi: 10.1016/j.tins.2016.05.002.
- Björn Rasch, Christian Büchel, Steffen Gais, Jan Born. Odor Cues During Slow-Wave Sleep Prompt Declarative Memory Consolidation // Science. 2007. V. 315. P. 1426–1429.
- McCarley RW. Neurobiology of REM and NREM sleep. Sleep Med. 2007 Jun;8(4):302–30. doi: 10.1016/j.sleep.2007.03.005. Epub 2007 Apr 30. PMID: 17468046.
- Оганесян Г.А., Аристакесян Е.А., Романова И.В., Ватаев С.И., Кузик В.В., Камбарова Д.К. Вопросы эволюции цикла бодрствование-сон. Часть 2: нейромедиаторные механизмы регуляции // Биосфера. 2013. № 1.
- Howell MJ, Schenck CH. Rapid Eye Movement Sleep Behavior Disorder and Neurodegenerative Disease. JAMA Neurol. 2015 Jun;72(6):707–12. doi: 10.1001/jamaneurol.2014.4563. PMID: 25867792
- Roguski A, Rayment D, Whone AL, Jones MW and Rolinski M (2020) A Neurologist„s Guide to REM Sleep Behavior Disorder. Front. Neurol. 11:610. doi: 10.3389/fneur.2020.00610
- Howell M, Avidan AY, Foldvary-Schaefer N, Malkani RG, During EH, Roland JP, McCarter SJ, Zak RS, Carandang G, Kazmi U, Ramar K. Management of REM sleep behavior disorder: an American Academy of Sleep Medicine clinical practice guideline. J Clin Sleep Med. 2023 Apr 1;19(4):759–768. doi: 10.5664/jcsm.10424. PMID: 36515157; PMCID: PMC10071384.
- Дамулин И.В. с соавт. Нейромидин в клинической практике. 2-с изд., перераб. и доп. — М.: ООО «Медицинское информационное агентство». 2016. — 60 с. ISDB 978–5-8948–1942–6.
- Sara V. Maurer, Christina L. Williams. «The Cholinergic System Modulates Memory and Hippocampal Plasticity via Its Interactions with Non-Neuronal Cells». Front. Immunol., 08 November 2017. DOI: 10.3389/fimmu.2017.01489.
- Kevin J. Tracey. «Physiology and Immunology of the Cholinergic Anti-inflammatory Pathway». J Clin Invest. 2007;117(2):289–296.
- Pavlov VA, Wang H, Czura CJ, Friedman SG, Tracey KJ. «The cholinergic anti-inflammatory pathway: A missing link in neuroimmunomodulation». Mol Med. 2003;9(5–8):125–134.
- Воробьева, О.В. Эффективность и безопасность препарата ноофен в терапии синдрома хронической усталости у больных с цереброваскулярной недостаточностью / О.В. Воробьева, В.В. Русая // Журнал неврологии и психиатрии им. C.C. Корсакова. — 2017. — Т. 117, № 11. — С. 31–36. — DOI 10.17116/jnevro201711711131–36. — EDN ZXGAJB.
- Инструкция по медицинскому применению лекарственного препарата Ноофен®.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Немного статистики о диабетической нейропатии
Какова, на Ваш взгляд, распространенность диабетической полинейропатии (ДПН) среди пациентов с длительным анамнезом сахарного диабета?


Нейропатическая боль снижает качество жизни пациентов:
- приводит к нарушению повседневной деятельности
- является причиной инвалидизации
- влияет на психосоциальные аспекты1
Что важно учитывать в патогенезе заболевания?
Ключевые пути повреждения при хронической гипергликемии объединены общим связующим звеном — окислительным стрессом.
Метаболический путь:
активация полиолового шунта ведет к накоплению сорбитола и истощению миоинозитола, а неферментативное гликирование белков нарушает функцию структур эндоневрия. Важнейшим следствием этих процессов является генерация активных форм кислорода (АФК) и мощный окислительный стресс2.
Сосудистый путь:
именно этот окислительный стресс, возникший в результате метаболических нарушений, является прямой причиной эндотелиальной дисфункции, провоцируя микроваскулярную недостаточность, ишемию и гипоксию нервного волокна2.


Стратегия восстановления под новым углом
Основными принципами ведения пациентов с ДПН остаются контроль гликемии, болевых ощущений, модификации образа жизни и регулярные осмотры специалистами3.
Какую актуальную поддержку мы можем предложить пациентам, испытывающим всю тягость заболевания?


Место Нейромидин® в современной парадигме терапии
Рациональным выбором является применение препаратов, направленных на патогенетическое звено — улучшение нервно-мышечной передачи. Нейромидин® (Ипидакрин) обладает тройным эффектом4:


Нейромидин®
Это не просто симптом-модифицирующий агент, а патогенетически обоснованный инструмент, обладающий рядом клинических преимуществ:


СД — сахарный диабет, ДПН — диабетическая полинейропатия, ADA — Американская диабетическая ассоциация, АФК — активные формы кислорода, ЭНМГ — электронейромиография
- Rodica Pop-Busui, Andrew J.M. Boulton, Eva L. Feldman, Vera Bril, Roy Freeman, Rayaz A. Malik, Jay M. Sosenko, Dan Ziegler; Diabetic Neuropathy: A Position Statement by the American Diabetes Association. Diabetes Care 1 January 2017; 40 (1): 136–154. https://doi.org/10.2337/dc16-2042
- Edwards JL, Vincent AM, Cheng HT, Feldman EL. Diabetic neuropathy: mechanisms to management. Pharmacol Ther. 2008 Oct;120(1):1-34. doi: 10.1016/j.pharmthera.2008.05.005. Epub 2008 Jun 13. PMID: 18616962; PMCID: PMC4007052.
- Elafros MA, Andersen H, Bennett DL, Savelieff MG, Viswanathan V, Callaghan BC, Feldman EL. Towards prevention of diabetic peripheral neuropathy: clinical presentation, pathogenesis, and new treatments. Lancet Neurol. 2022 Oct;21(10):922-936. doi: 10.1016/S1474-4422(22)00188-0. PMID: 36115364; PMCID: PMC10112836.
- Инструкция по медицинскому применению лекарственного препарата Нейромидин® (ЛСР-008102/10). Дата обращения 23.09.2025.
- Данилов А.Б., Амелин А.В. Периферические нейропатии с расстройством чувствительности: нейробиологические аспекты нейрорегенерации. Manage Pain. 2023;3:20-24.
- Ромейко Д.И., и др. Эффективность применения Нейромидина в терапии диабетической дистальной полинейропатии. Медицинские новости. 2009;6:2-3.
- Levin O.S., et al. Modern principles of diagnosis and treatment of polyneuropathies. Sovremennaya terapiya v psikhiatrii i nevrologii. 2021;(3-4):46-55.
- Korobkova DZ, Maksimova MYu, Sineva NA, Vodop’ianov NP, Mikhal’chenko VN. Neyromidin in ischemic stroke. S.S. Korsakov Journal of Neurology and Psychiatry. 2013;113(3):34‑38.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
Хронический тонзиллит (ХТ) необходимо рассматривать, как очаговую инфекцию, элиминация которой является необходимой частью стратегии сохранения здоровья человека в целом и кардинальном лечении имеющихся сопряженных заболеваний [1-4]. На сегодняшний день различными специалистами отмечается рост осложнений, связанных с заболеваниями небных миндалин (НМ). С течением десятилетий ситуация кардинально не изменилась – количество тонзиллэктомий (ТЭ) уменьшилось в 10 раз, а развитие декомпенсированных форм ХТ возросло в 5 раз [5, 6].
Создавшаяся ситуация неотвратимо ведет к значимым экономическим затратам и резкому снижению качества жизни (КЖ) пациентов.
Как правило, ХТ болеют дети и лица молодого, наиболее работоспособного возраста. С данной проблемой пациенты обращаются не только к оториноларингологу, но и к врачам общей практики, терапевтам, педиатрам и прочим специалистам. ХТ представляет собой не узкоспецифическую оториноларингологическую патологию, а междисциплинарную проблему.
Источник: Саливончик Е.И. Монография «Избранные вопросы оториноларингологии для врача общей практики»
Поллиноз (от лат. pollen — пыльца) – одно из самых распространенных аллергических заболеваний, вызываемое пыльцой растений. Наиболее часто первые симптомы заболевания проявляются в возрасте 3-9 лет. Клинические проявления поллиноза обусловлены воспалительными изменениями слизистой оболочки, в основном глаз и дыхательных путей. Заболевание имеет четкую сезонность, повторяющуюся из года в год, совпадающую с периодом цветения тех или иных растений. В основном это ветроопыляемые растения, выделяющие огромные количества мелкой (0.02-0.04 мм) пыльцы, переносимой ветром на большие расстояния. Кроме определенного размера, пыльца должна обладать летучестью и сосредотачиваться в воздухе в значительных количествах (лишь около 50 растений продуцируют пыльцу, которая может вызывать поллиноз). У большинства страдающих поллинозом аллергия развивается на определенные виды растений. В свою очередь, растения выбрасывают пыльцу в воздух в течение 1-2-х месяцев — это и есть средняя продолжительность обострения поллиноза. Однако при наличии сенсибилизации к нескольким видам растений клинические симптомы заболевания могут продолжаться и более длительное время.
В РБ выделяют три основных периода цветения: весенний (апрель–май), когда в воздухе присутствует пыльца деревьев (береза, ольха, дуб, орешник и др.), летний (июнь–июль), обусловленный пыльцой злаковых трав (райграс, ежа, костер, тимофеевка мятлик, пырей, овсяница, лисохвост и др.), и летне-осенний (август–октябрь), связанный с цветением сорных трав (полынь, лебеда, амброзия).
Примерный календарь цветения деревьев и трав средней полосы
| ВИД РАСТЕНИЯ | СРОКИ ЦВЕТЕНИЯ |
| ольха, орешник, ива, вяз | 15-30 апреля |
| осина, тополь | 15-30 апреля |
| береза, клен | 1-20 мая |
| сосна | 25 мая — 5 июня |
| одуванчик | 5-15 июня |
| костер, лисохвост | 5-26 июня |
| липа | 20 июня — 5 июля |
| дуб | 22-24 мая |
| овсяница, ежа, пырей | 5-25 июля |
| тимофеевка, мятлик | 5-25 июля |
| полынь, амброзия, лебеда | 1-15 сентября |
Следует учитывать, что в зависимости от метеорологических условий сроки цветения растений могут на 7-14 дней отклоняться от календарных
Клинические проявления поллиноза
Наиболее типичное проявление поллиноза – риноконъюнктивальный синдром: слезотечение, светобоязнь, выраженная гиперемия конъюнктив, резкий зуд и отек век, ощущение «песка» в глазах в сочетании с затруднением носового дыхания, зудом в носу и носоглотке, приступами чихания с обильным жидким прозрачным отделяемым. Реже встречается поражение слизистой нижних дыхательных путей с появлением клинических симптомов астмы: приступы удушья, свистящие хрипы, слышные на расстоянии, сухой кашель. К еще более редким проявлениям пыльцевой аллергии относятся крапивница, отек Квинке, а также сезонные пыльцевые дерматиты, особенностью которых является тяжелое течение, изнуряющий зуд. Кроме органной симптоматики, у большинства больных в период обострения поллиноза отмечаются головные боли, потливость, общая слабость, бессонница. Температура тела чаще остается нормальной, у некоторых больных она может повышаться с последующим сохранением длительного субфебрилитета.
Диагностика поллиноза
Клиническая диагностика поллиноза основана на наличии типичных сезонных (весна-лето) симптомов аллергического ринита, поражения глаз, приступов бронхиальной астмы, кожных изменений, а также их повторяемости из года в год. В зависимости от спектра сенсибилизации клинические симптомы выражены в большей степени в период пыления причинно-значимых растений. Основной метод диагностики поллиноза — проведение кожных проб с пыльцевыми аллергенами, однако он проводится вне сезона цветения. В любой период заболевания для определения спектра сенсибилизации возможно определение специфических антител к пыльцевым аллергенам (диагностика in vitro).
Лечение поллиноза
Программа лечения больного поллинозом должна включать:
- Элиминационные мероприятия.
- Диетотерапию.
- Медикаментозную терапию.
- Аллергенспецифическую иммунотерапию.
Элиминационные мероприятия
Больным поллинозом в период пыления причинно-значимых растений рекомендуется избегать посещения загородной зоны (лес, луг), парков и скверов в городе. Необходимо занавешивать форточки мокрыми марлей или тканью, что уменьшает поступление пыльцы в жилище, окна и двери помещений держать по возможности закрытыми, проветривайте помещение после дождя, вечером, когда концентрация пыльцы в атмосфере минимальная, ежедневно проводить влажную уборку, использовать очистители воздуха или кондиционеры. Выходя на прогулку, целесообразно защищать глаза плотно прилегающими очками, использовать барьерные средства для защиты слизистой оболочки носа, а после возвращения с улицы следует поменять одежду, принять душ, прополоскать рот, промыть глаза. При аллергическом поражении кожи рекомендуется носить одежду с длинными рукавами и длинные брюки. В квартире не следует ставить букеты живых и сухих цветов, разводить цветущие растения.
Диетотерапия
Детям с поллинозами не рекомендуется применять фитопрепараты и мед. Также у части пациентов при употреблении в пищу некоторых продуктов питания могут появляться симптомы аллергии в виде зуда в полости рта, отека языка, першения в горле, проявления ринита и конъюнктивита. Эта разновидность аллергии называется перекрестной и связана с тем, что белки в пыльце и некоторые пищевые продукты могут быть структурно схожими, что заставляет иммунную систему путать их и вызывать аллергическую реакцию. Такая реакция отмечается у 60% детей с поллинозом и требует исключения данных продуктов из рациона.
Перекрестная пищевая аллергия
| Сенсибилизация | Пищевые продукты, вызывающие перекрестные аллергические реакции |
| Сенсибилизация к пыльце деревьев | Орехи, яблоки, груша, черешня, персики, слива, киви, морковь, петрушка, сельдерей, помидоры |
| Сенсибилизация к пыльце злаковых трав | Хлеб и хлебобулочные изделия, каши, макароны, продукты из злаков, клубника, земляника, цитрусовые, соя, бобы, арахис, кукуруза |
| Сенсибилизация к пыльце сорных трав | Семена подсолнечника, подсолнечное масло, халва, горчица, майонез, цикорий, дыня, арбуз, зелень и специи (петрушка, укроп, корица, тмин, кари, перец, анис, имбирь) |
Медикаментозная терапия. Рекомендуется в сезон цветения использование 0,9 % раствора натрия хлорида для регулярного промывания слизистой полости носа. Для купирования симптомов поллиноза используют неседативные антигистаминные препараты (например, хифенадин и др.) и топические (интраназальные) стероиды. Симптоматическое лечение аллергического ринита включает также кратковременное (5-6 дней) использование сосудосуживающих препаратов, так как длительная терапия приводит к нарушению микроциркуляции в слизистой оболочке носа и формированию медикаментозного ринита.
Аллергенспецифическая иммунотерапия (АСИТ). При выявлении причинно-значимого аллергена и высокой степени сенсибилизации проводится иммунотерапия аллергенными вакцинами. Данный метод лечения направлен на формирование иммунологической толерантности (потере чувствительности) к пыльцевым аллергенам. АСИТ является единственным этиопатогенетическим методом лечения аллергических заболеваний, заключающимся во введении постепенно возрастающих количеств аллергена пациенту. Вводят аллергены подкожно или сублингвально (под язык). Иммунотерапия аллергенами показана детям старше 5 лет с поллинозом в периоде ремиссии заболевания и проводится врачом-аллергологом. Лечение проводится ежегодно на протяжении 3-5 лет.
Автор статьи: Буза Дмитрий Викторович, врач-аллерголог высшей категории, к.м.н.
Цель исследования – определить микробный пейзаж у пациентов с острыми и хроническими воспалительными заболеваниями глотки в период пандемии новой коронавирусной инфекции COVID-19 и сравнить с «доковидным» периодом.
Материал и методы исследования
Проведено ретроспективное сплошное одномоментное исследование бактериологических анализов образцов отделяемого из глотки у группы пациентов, обратившихся к оториноларингологу на амбулаторный прием с жалобами на боль в горле при установленном диагнозе острого и обострения хронического заболевания глотки в период новой коронавирусной инфекции COVID-19 (основная группа, n=308, 2020-2022 годы). Группу сравнения (n=95, 2019 год) составили результаты бактериологического исследования у пациентов с аналогичной патологией в «доковидный» период.
Источник: Саливончик Е.И. Монография «Избранные вопросы оториноларингологии для врача общей практики»
Хронический дефицит сна в современном мире превратился в массовую проблему со множественными негативными последствиями для здоровья.
Дефицит сна — эпидемия XXI века?
Современные исследования показывают тревожную статистику распространенности инсомнии среди различных групп населения, что делает эту проблему приоритетной для системы здравоохранения1.
- Бессонница чаще встречается у пожилых людей, при этом общая распространенность составляет 20%1
- Примерно у трети взрослых наблюдается один или несколько симптомов дефицита сна1
- Женщины в 1,2-1,4 раза чаще страдают бессонницей1


В основе инсомнии лежат сложные биохимические и нейрофизиологические процессы, отражающие взаимодействие различных отделов ЦНС 2,3. Патофизиологические механизмы, определяющие развитие инсомнии:
- Дисбаланс нейротрансмиттеров (возбуждающих и тормозных)2,3
- Снижение концентрации ГАМК2,3
- Депривация сна индуцирует изменения в сигнальных путях, экспрессии генов и может вызывать изменения в дендритной структуре нейронов2,3


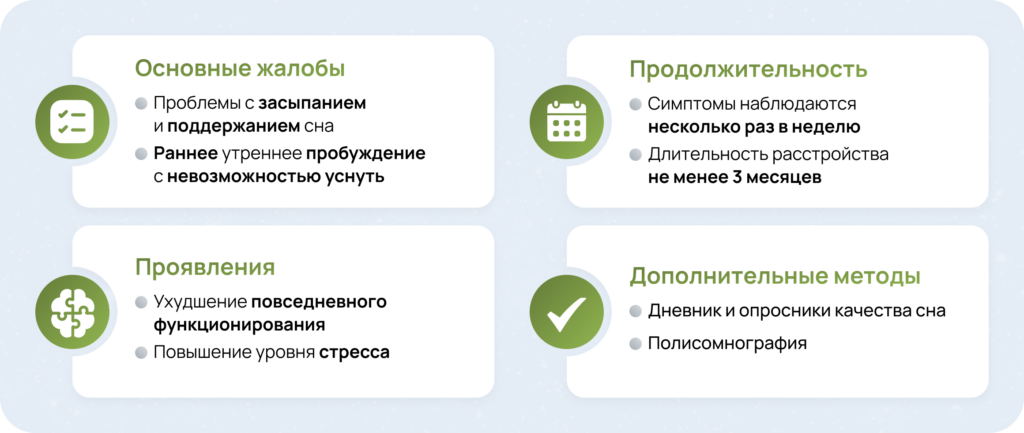
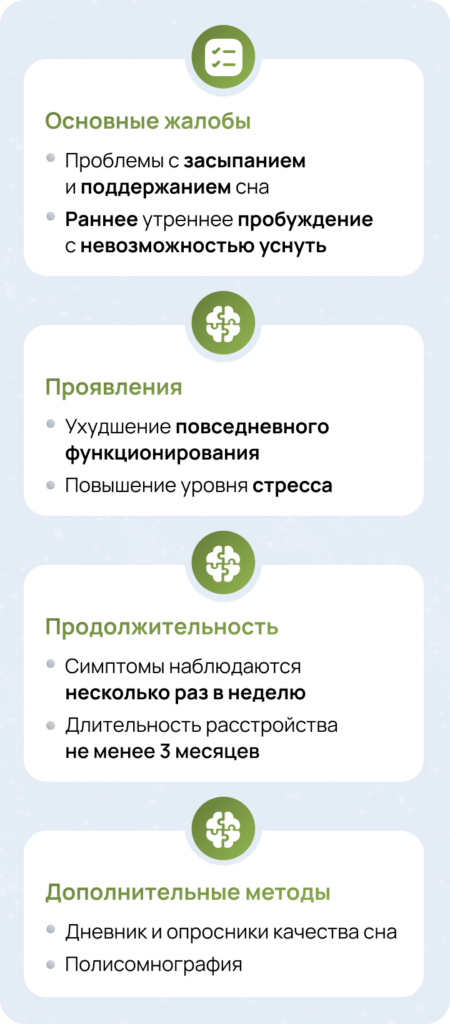
Комплексная диагностика инсомнии4
Точная диагностика инсомнии требует систематического подхода и оценки множества параметров. Необходимо учитывать не только жалобы пациента, но и характеристики расстройства, его продолжительность и влияние на качество жизни.
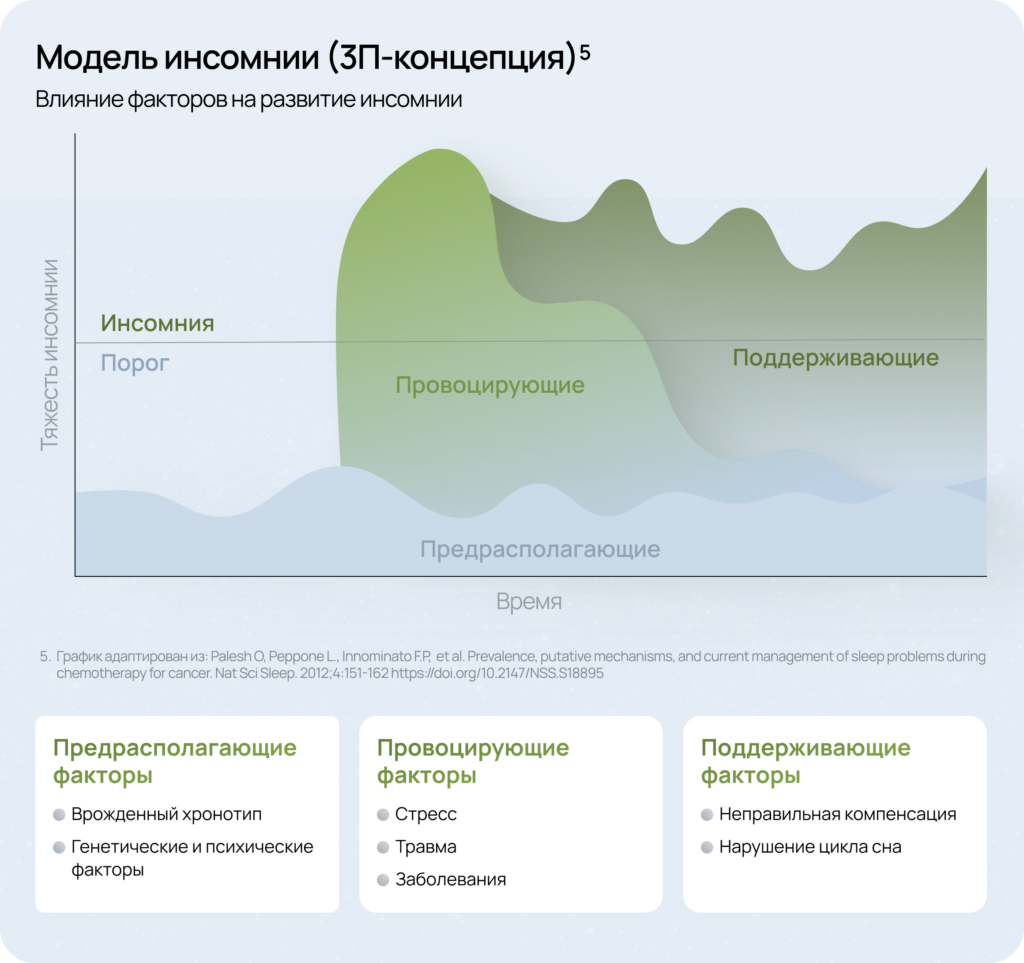
Для понимания механизмов развития и хронизации инсомнии широко применяется модель трех факторов (3П-концепция), которая помогает идентифицировать ключевые точки терапевтического воздействия и разработать персонализированный план ведения пациента5.

Подходы к терапии инсомнии4
Современный подход к лечению инсомнии включает немедикаментозную и медикаментозную терапию. Выбор терапевтической стратегии должен основываться на индивидуальных особенностях пациента, тяжести расстройства и наличии сопутствующих заболеваний.
- Когнитивно-поведенческая терапия. Направлена на ментальные или когнитивные аспекты бессонницы и восстановление здорового режима сна. Может проводиться индивидуально или в группах.
- Медикаментозная терапия. Назначение седативных препаратов различных групп для улучшения качества сна. Краткосрочная терапия (≤ 4 недель).
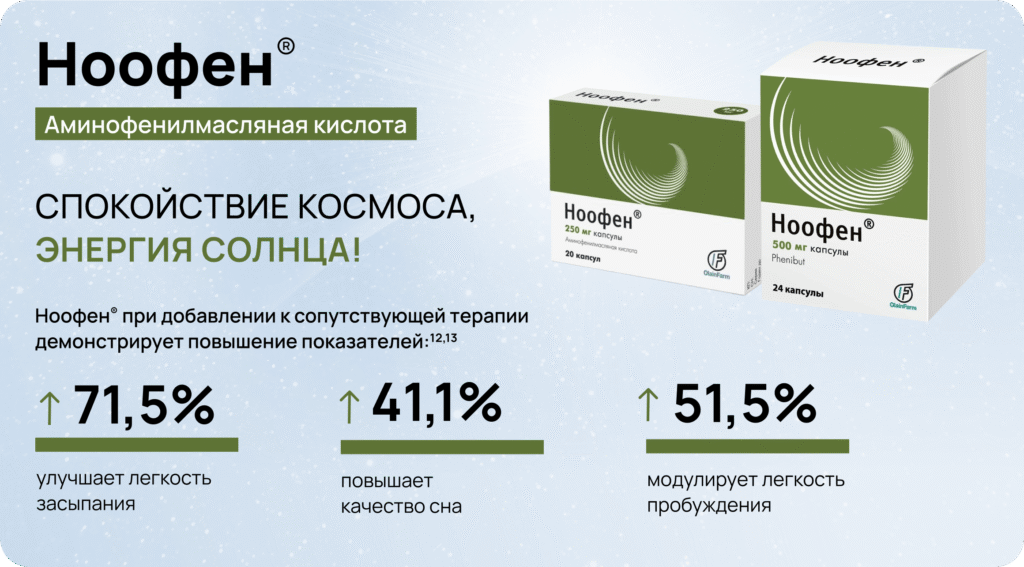
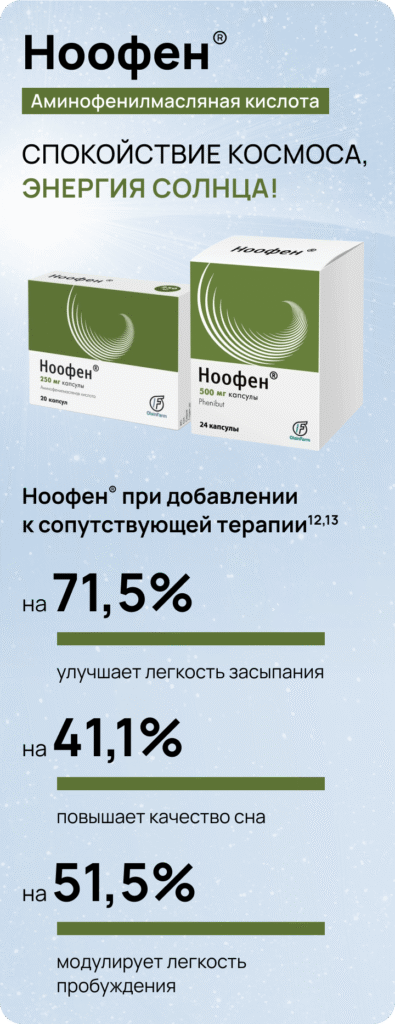
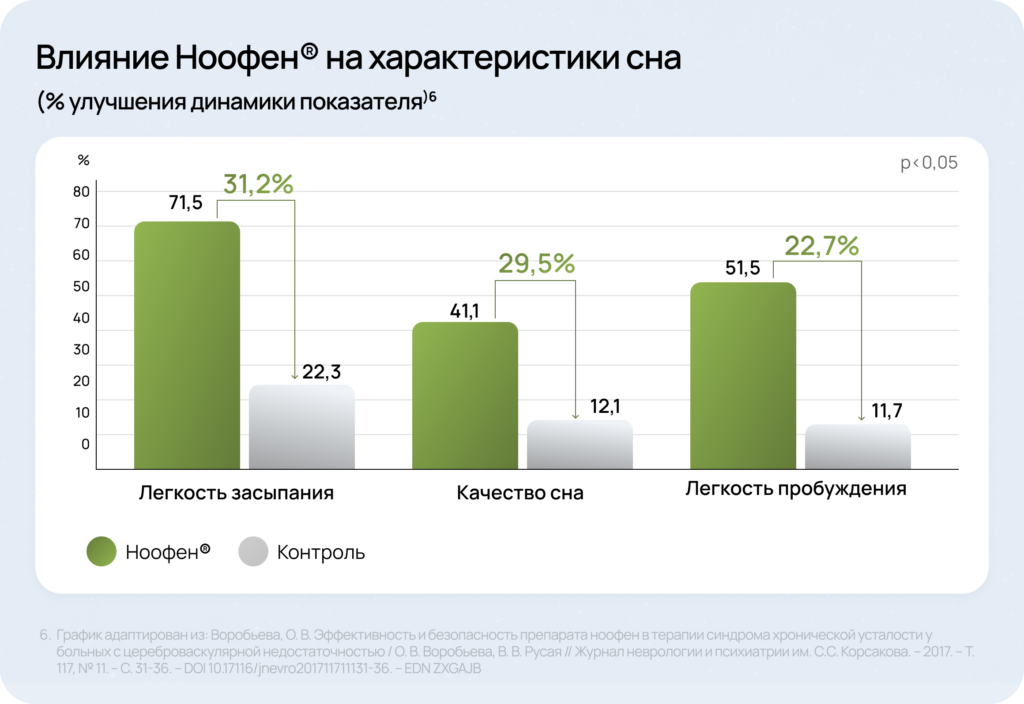
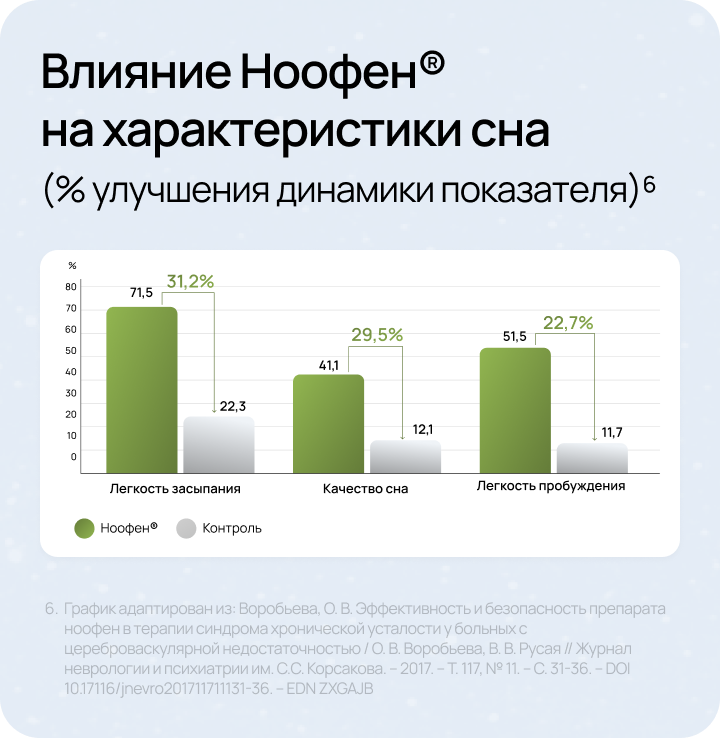
Оптимальным решением для медикаментозной терапии может выступать аминофенилмасляная кислота (например, препарат Ноофен®)6.




ЦНС — центральная нервная система
ГАМК — гамма-аминомасляная кислота
- Risk factors, comorbidities, and consequences of insomnia in adults [Электронный ресурс] // UpToDate. URL: https://www.uptodate.com/contents/risk-factors-comorbidities-and-consequences-of-insomnia-in-adults (дата обращения: 01.11.2025).
- Varinthra, P., Anwar, S. N. M. N., Shih, S. C., & Liu, I. Y. (2024). The role of the GABAergic system on insomnia. Tzu chi medical journal, 36(2), 103–109. https://doi.org/10.4103/tcmj.tcmj_243_23.
- Lyons, L. C., Vanrobaeys, Y., & Abel, T. (2023). Sleep and memory: The impact of sleep deprivation on transcription, translational control, and protein synthesis in the brain. Journal of neurochemistry, 166(1), 24-46. https://doi.org/10.1111/jnc.15787.
- Riemann D, Espie CA, Altena E, Arnardottir ES, Baglioni C, Bassetti CLA, Bastien C, Berzina N, Bjorvatn B, Dikeos D, Dolenc Groselj L, Ellis JG, Garcia-Borreguero D, Geoffroy PA, Gjerstad M, Gonçalves M, Hertenstein E, Hoedlmoser K, Hion T, Holzinger B, Janku K, Jansson-Fröjmark M, Järnefelt H, Jernelöv S, Jennum PJ, Khachatryan S, Krone L, Kyle SD, Lancee J, Leger D, Lupusor A, Marques DR, Nissen C, Palagini L, Paunio T, Perogamvros L, Pevernagie D, Schabus M, Shochat T, Szentkiralyi A, Van Someren E, van Straten A, Wichniak A, Verbraecken J, Spiegelhalder K. The European Insomnia Guideline: An update on the diagnosis and treatment of insomnia 2023. J Sleep Res. 2023 Dec;32(6):e14035. doi: 10.1111/jsr.14035. PMID: 38016484.
- Palesh O, Peppone L., Innominato F.P, et al. Prevalence, putative mechanisms, and current management of sleep problems during chemotherapy for cancer. Nat Sci Sleep. 2012;4:151-162 https://doi.org/10.2147/NSS.S18895.
- Воробьева, О. В. Эффективность и безопасность препарата ноофен в терапии синдрома хронической усталости у больных с цереброваскулярной недостаточностью / О. В. Воробьева, В. В. Русая // Журнал неврологии и психиатрии им. C.C. Корсакова. — 2017. — Т. 117, № 11. — С. 31-36. — DOI 10.17116/jnevro201711711131-36. — EDN ZXGAJB.
- Инструкция по медицинскому применению препарата Ноофен®, капсулы 500 мг.
- Vlasov, N. A. «Effect of Derivatives of Gamma-Aminobutyric Acid on Sleep Disturbances in Neuroses.» Bulletin of Experimental Biology and Medicine, vol. 85, no. 2, 1978, pp. 169-171
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
IgE‑независимая реакция, обусловленная снижением активности фермента диаминоксидазы (DAO), синтезируемого клетками тонкого кишечника, и приводящая к повышению уровня гистамина в организме после приема богатой гистамином пищи, алкоголя, ряда лекарственных препаратов.
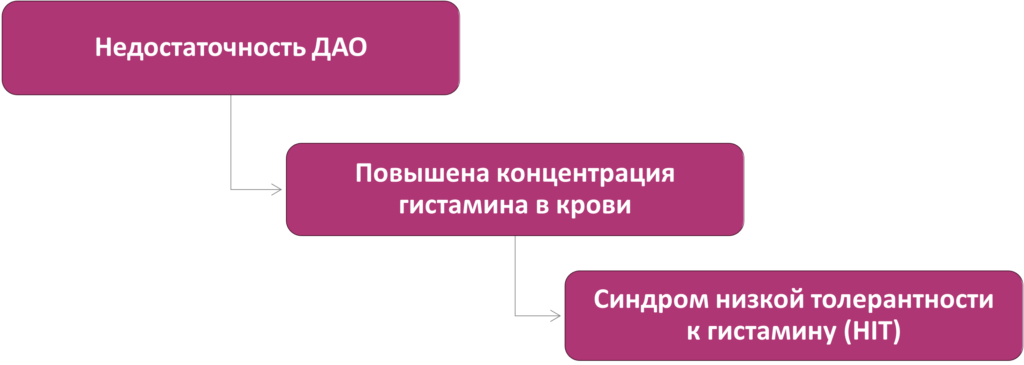

При употреблении продуктов, повышающих концентрацию гистамина в организме (ферментированные продукты (сыры, квашеная капуста), копчености, переработанные мясные продукты(сосиски, колбасы), морепродукты, рыба скумбрия, сельдь, тунец (особенно консервированная), высокобелковые продукты (белок куриного яйца), дрожжи, алкоголь (красное вино, пиво), кисломолочные продукты, продуктов либераторов гистамина-цитрусовые, клубника, шоколад, какао, орехи, папайя, ананас, помидоры, шпинат, пищевые добавки; продуктов, блокирующих DAO: черный и зеленый чай, энергетические напитки) через 10-15 минут возникает целый комплекс симптомов со стороны кожных покровов – покраснение, волдыри, зуд, отечность, чувство жара, со стороны желудочно-кишечного тракта (боль, метеоризм, диарея, тошнота, рвота, изжога), головная боль, со стороны дыхательной системы (ринорея, заложенность носа, бронхоспазм, затрудненное дыхание) и другие симптомы.
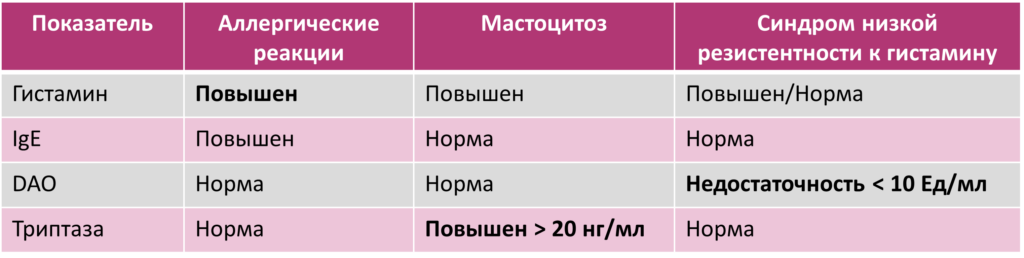
Таблица 1. Дифференциальная диагностика синдрома низкой резистентности к гистамину
Фармакотерапия
- Заместительная терапия препаратами DAO. Принимаются перорально непосредственно перед едой. Могут значительно уменьшить симптомы, связанные с приемом пищи.
- Антигистаминные препараты (блокаторы H1- и H2-рецепторов). Купируют симптомы, но не влияют на причину. При этом, в отличие от других Н1 блокаторов, Хифенадин Фенкарол обладает особым механизмом действия: не только блокирует гистаминовые Н1-рецепторы в периферических тканях, но и активирует фермент DAO, который разрушает гистамин в тканях. Именно поэтому Хифенадин Фенкарол начинает действовать очень быстро, и именно этим объясняется эффективность Хифенадин Фенкарола для больных, лечение которых другими антигистаминными средствами неэффективно. H2-блокаторы (фамотидин) особенно эффективны при желудочно-кишечных симптомах.
- Также применяют Стабилизаторы мембран тучных клеток — кромоглициевая кислота.
- Кортикостероиды — только в тяжелых случаях, коротким курсом.
- Важным элементом лечения является коррекция сопутствующей патологии: лечение заболеваний ЖКТ, нормализация микробиоты, терапия SIBO.
- Восполнение дефицита кофакторов (витамин B6, витамин C, медь).
- Повышение активности фермента DAO можно добиться с помощью приема препаратов аскорбиновой кислоты, пиридоксина, цинка, магния.
- Положительный клинический эффект достигается от применения низкогистаминовой диеты.
Автор: Надежда Дмитриевна Титова, доктор медицинских наук, доцент, врач-педиатр, врач-аллерголог-иммунолог
Тики и заикания относятся к числу наиболее распространенных неврологических расстройств у детей, которые существенно влияют на качество жизни, развитие коммуникационных навыков и социальную адаптацию1,2.
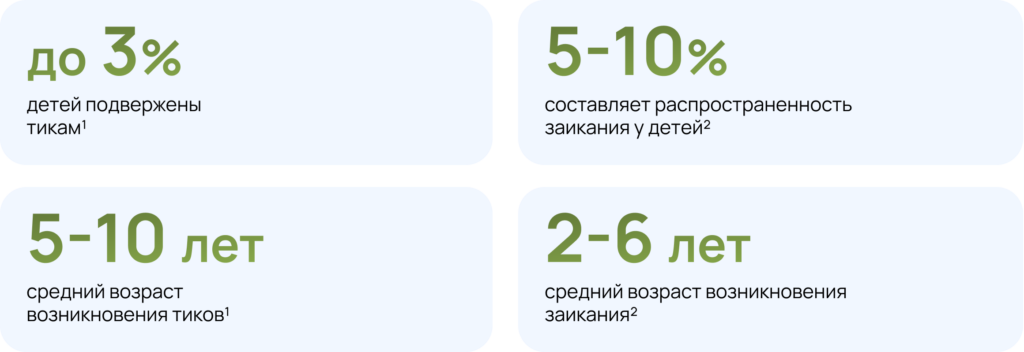

К причинам развития тиков и заикания у детей относится дисфункция дофаминергической системы, генетическая предрасположенность, стресс и тревожность1,2.


Совершенствование методов диагностики позволяет точно определять формы тиковых расстройств5

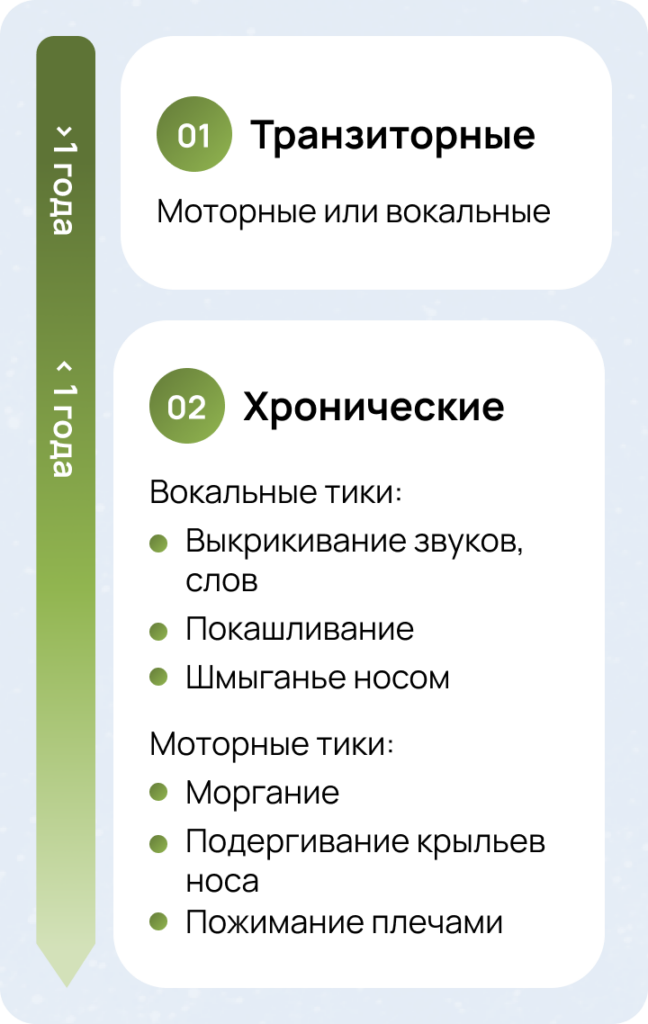
Систематизация диагностической классификации согласно DSM-5 обеспечивает стандартизированный подход, облегчающий клиническую оценку3.

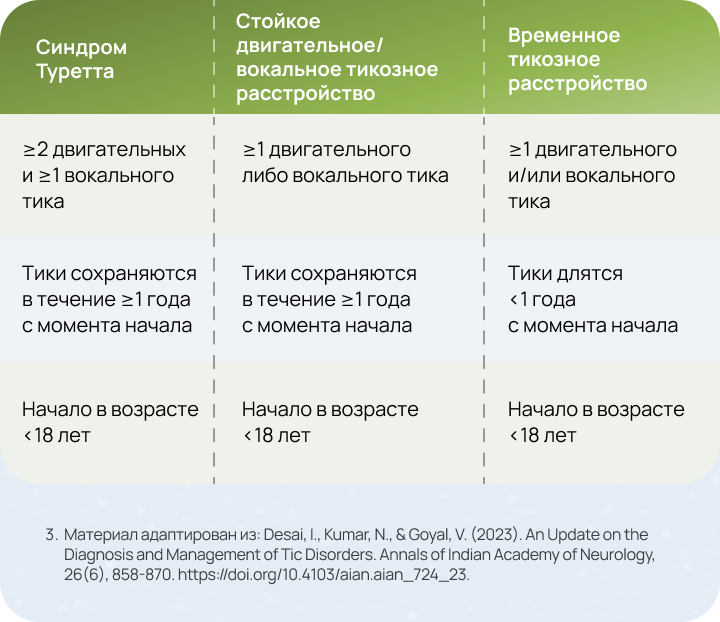
Также важно понимать сенсорные и психосоматические особенности, сопровождающие тики, так как они существенно влияют на выбор терапии3.
- Продромальные позывы: неприятные ощущения, возникающие перед началом тика и исчезающие сразу после него. Могут быть соматическими (зуд) и психосоматическим (чувство беспокойства).
- Повышенная чувствительность к внешним и внутренним раздражителям: зрительным, тактильным, слуховым и обонятельным.
- Способность к произвольному подавлению тиков: сильное подавление может усилить выраженность продромальных позывов.
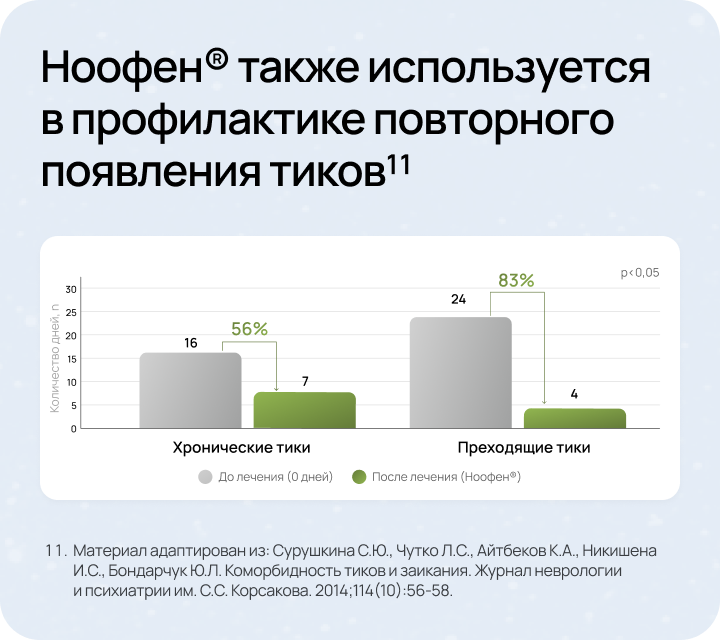
Современная стратегия лечения тиков у детей основывается на комбинированном подходе, сочетающем психотерапевтические и медикаментозные методы.
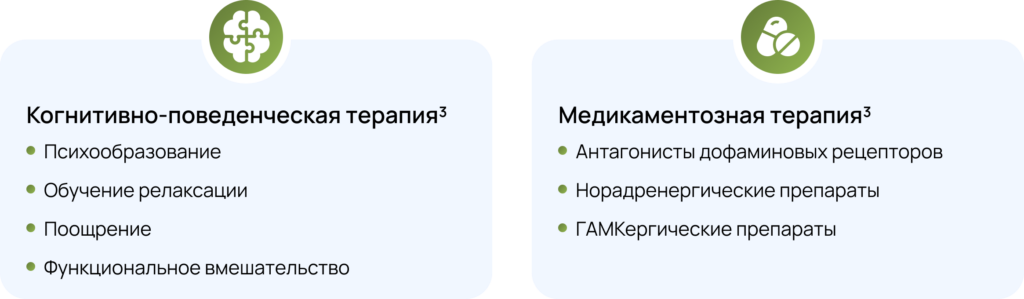

Комплексный подход к лечению заикания у детей
Недавние исследования расширили представление о патофизиологических основах заикания у детей. Комплексный научный подход позволяет выявлять не только биологические, но и психосоциальные, генетические и гендерные факторы риска:




Лечение заикания у детей включает фармакологическую и немедикаментозную коррекцию, направленную на снятие психологического напряжения и коррекцию речи.




После лечения препаратом Ноофен® отмечено:

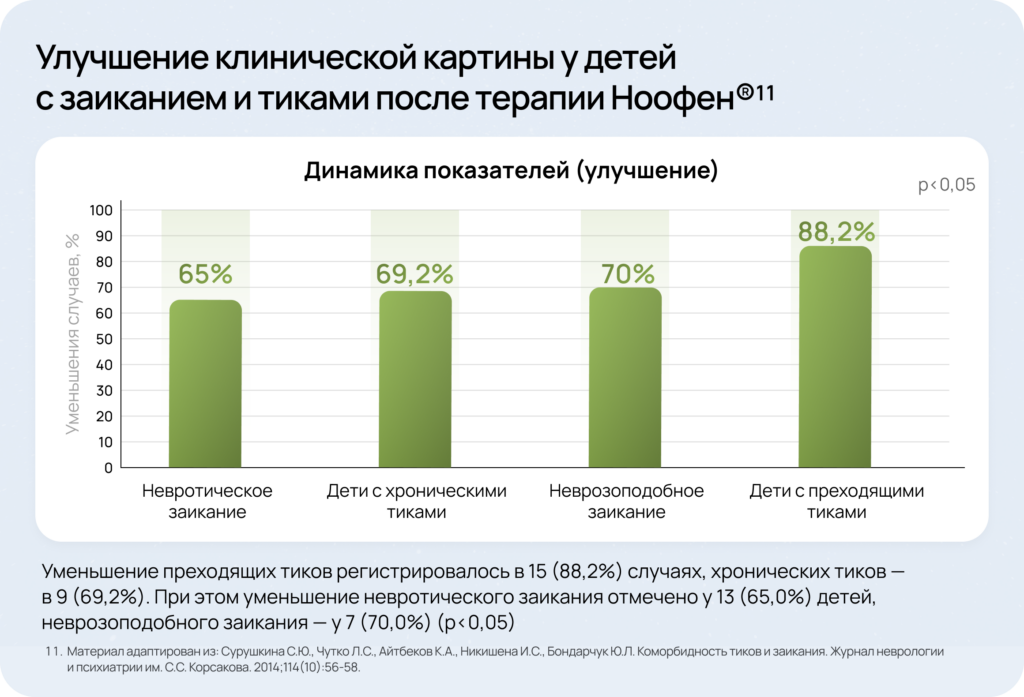
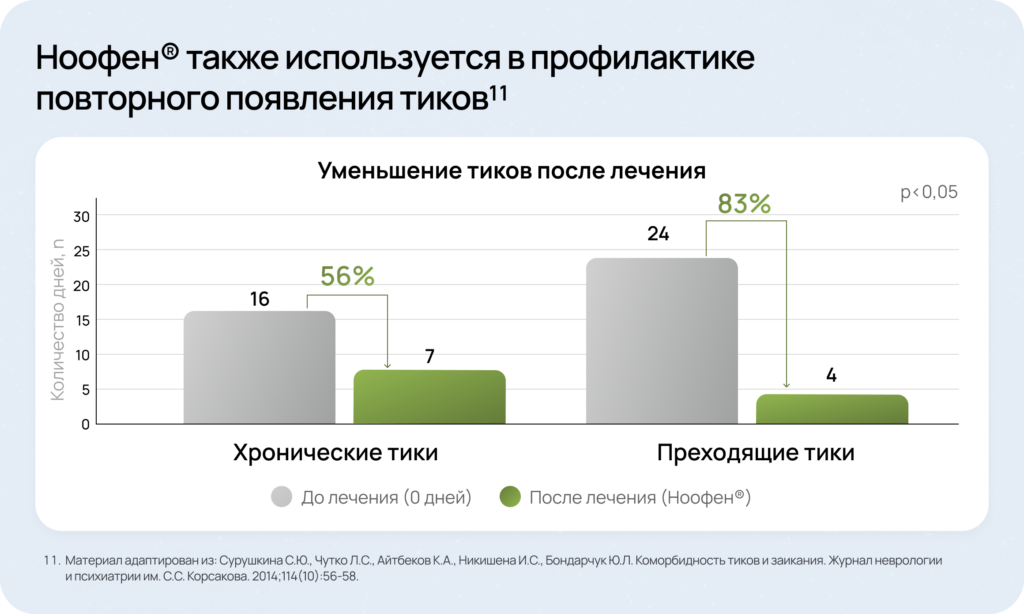


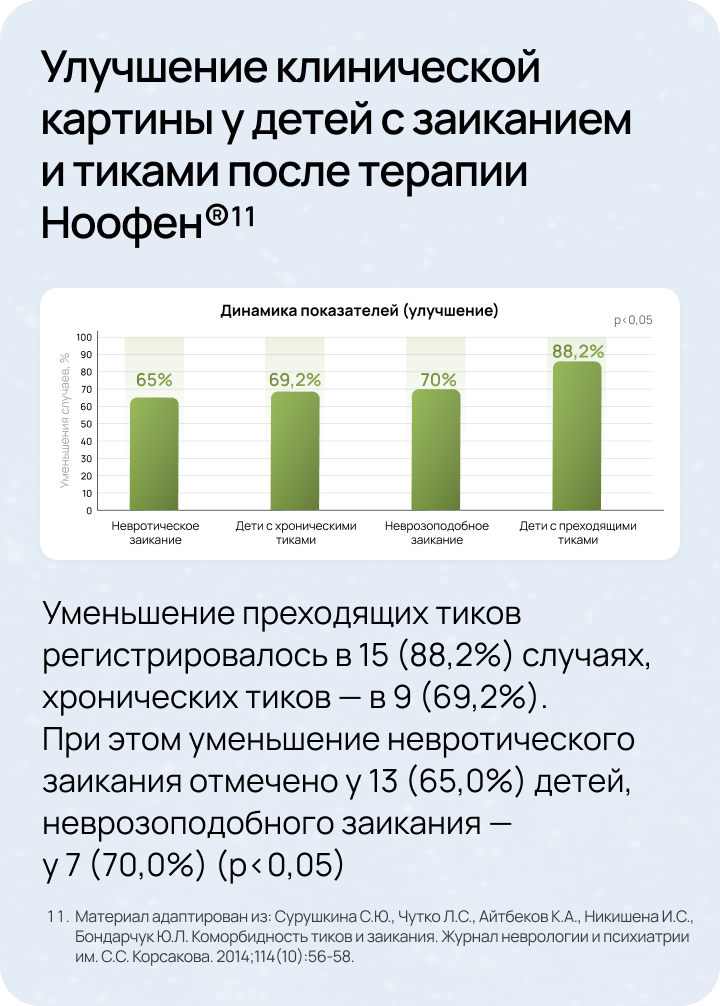

DSM-5 — Диагностическое и статистическое руководство по психическим расстройствам, 5-е издание. SSI — Тест определения степени заикания. BAB — Система оценки поведения. OASES — Тест общей оценки заикания.
- Tang, N., Wang, Y., Jiang, X., Liu, H., Li, Y., Qu, J., & Xiang, S. (2025). Clinical characteristics of tic disorders in children and adolescents with the chief complaint of abnormal blinking. Frontiers in psychiatry, 16, 1553358. https://doi.org/10.3389/fpsyt.2025.1553358.
- Hussain SAS, Lui F. Stuttering (Stammering) [Updated 2024 Apr 17]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK603738/.
- Desai, I., Kumar, N., & Goyal, V. (2023). An Update on the Diagnosis and Management of Tic Disorders. Annals of Indian Academy of Neurology, 26(6), 858-870. https://doi.org/10.4103/aian.aian_724_23.
- Hartmann, A., Andrén, P., Atkinson-Clement, C., Czernecki, V., Delorme, C., Mol Debes, N., Morand-Beaulieu, S., Müller-Vahl, K., Paschou, P., Szejko, N., Topaloudi, A., & Black, K. J. (2024). Tourette syndrome research highlights from 2023. F1000Research, 13, 677. https://doi.org/10.12688/f1000research.150931.2.
- Cohen, S. C., Leckman, J. F., & Bloch, M. H. (2013). Clinical assessment of Tourette syndrome and tic disorders. Neuroscience and biobehavioral reviews, 37(6), 997-1007. https://doi.org/10.1016/j.neubiorev.2012.11.013.
- Polikowsky, H.G., Scartozzi, A.C., Shaw, D.M. et al. Large-scale genome-wide analyses of stuttering. Nat Genet 57, 1835-1847 (2025). https://doi.org/10.1038/s41588-025-02267-2.
- Neef, N. E., & Chang, S. E. (2024). Knowns and unknowns about the neurobiology of stuttering. PLoS biology, 22(2), e3002492. https://doi.org/10.1371/journal.pbio.3002492.
- Asci F, Marsili L, Suppa A, Saggio G, Michetti E, Di Leo P, Patera M, Longo L, Ruoppolo G, Del Gado F, Tomaiuoli D and Costantini G (2023) Acoustic analysis in stuttering: a machine-learning study. Front. Neurol. 14:1169707. doi: 10.3389/fneur.2023.1169707.
- Pertijs, M.A.J., Oonk, L.C., Beer, de J.J.A., Bunschoten, E.M., Bast, E.J.E.G., Ormondt, van J., Rosenbrand, C.J.G.M., Bezemer, M., Wijngaarden, van L.J., Kalter, E.J., Veenendaal, van H. (2014). Clinical Guideline Stuttering in Children, Adolescents and Adults. NVLF, Woerden.
- Maguire, G. A., Nguyen, D. L., Simonson, K. C., & Kurz, T. L. (2020). The Pharmacologic Treatment of Stuttering and Its Neuropharmacologic Basis. Frontiers in neuroscience, 14, 158. https://doi.org/10.3389/fnins.2020.00158.
- Сурушкина С.Ю., Чутко Л.С., Айтбеков К.А., Никишена И.С., Бондарчук Ю.Л. Коморбидность тиков и заикания. Журнал неврологии и психиатрии им. С.С. Корсакова. 2014;114(10):56‑58.
- Инструкция по медицинскому применению препарата Ноофен®, капсулы 500 мг.
ИНФОРМАЦИЯ ДЛЯ СПЕЦИАЛИСТОВ ЗДРАВООХРАНЕНИЯ, НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО МЕДИЦИНСКОМУ ПРИМЕНЕНИЮ
